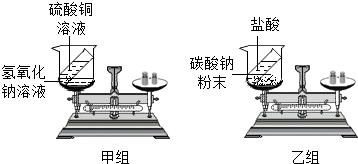
题目内容
超市卖的纯碱样品中往往会含有少量氯化钠,化学兴趣小组的同学要通过实验测定某品牌的纯碱样品中纯碱的质量分数.他们称取了15g样品,加水完全溶解后,向其逐滴加入稀盐酸,当加入的稀盐酸的质量为20g,40g,60g,时,生成气体的质量见下表.
试分析计算:
(1)第二组数据m为 .
(2)样品中纯碱的质量分数是多少?(精确到0.1g)
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀盐酸的质量/g | 20 | 40 | 60 |
| 生成气体的质量/g | 2.2 | m | 5.5 |
(1)第二组数据m为
(2)样品中纯碱的质量分数是多少?(精确到0.1g)
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:氯化钠不能和稀盐酸反应,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
根据二氧化碳的质量可以计算碳酸钠的质量,进一步可以计算样品中纯碱的质量分数.
根据二氧化碳的质量可以计算碳酸钠的质量,进一步可以计算样品中纯碱的质量分数.
解答:解:(1)由表中数据可知,加入20g稀盐酸时生成2.2g二氧化碳,加入60g时生成5.5g二氧化碳,说明加入60g稀盐酸时稀盐酸过量,加入40g时稀盐酸完全反应,生成的二氧化碳质量是4.4g.
故填:4.4;
(2)设碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 44
x 5.5g
=
,
x=13.25g,
样品中纯碱的质量分数为:
×100%=88.3%,
答:样品中纯碱的质量分数为88.3%.
故填:4.4;
(2)设碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 44
x 5.5g
| 106 |
| x |
| 44 |
| 5.5g |
x=13.25g,
样品中纯碱的质量分数为:
| 13.25g |
| 15g |
答:样品中纯碱的质量分数为88.3%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
下列实验操作正确是( )
A、 |
B、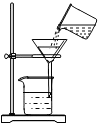 |
C、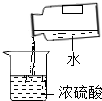 |
D、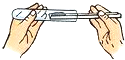 |
在某物质的饱和溶液中,挂一块该物质的缺角晶体,过一段时间后,该晶体( )
| A、无任何变化 |
| B、晶体的质量发生变化 |
| C、晶体溶解 |
| D、晶体质量不变,但形状变了 |
在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:下列说法中不正确的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 25 |
| 反应后质量/g | 未测 | 21 | 10 | 9 |
| A、该反应遵守质量守恒定律 |
| B、该反应为分解反应 |
| C、X中未测值为0 |
| D、若Q为氧气,则该反应为氧化还原反应 |
物质的用途与性质密切相关.下列说法不正确是( )
| A、氮气常用作保护气,是由于氮气的化学性质稳定 |
| B、二氧化碳通常用于灭火,是由于二氧化碳不可燃、不助燃且密度比空气大 |
| C、氧化钙可做食品干燥剂,氧化钙能与水反应 |
| D、因为铝的化学性质比较稳定,所以可用“银粉漆(铝粉)”涂在铁栏杆表面防锈 |