题目内容
11.实验室配制100g溶质质量分数为16%的氯化钠溶液.如图是小明的实验操作过程示意图:
(1)配制时需称量氯化钠16g,水84mL.
(2)图①中玻璃棒搅拌的目的是加快溶解速率.
(3)图中有一处明显的错误操作是③(填序号),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序⑤③④②①.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(2)根据溶解操作中玻璃棒的作用,进行分析解答.
(3)根据托盘天平的使用要遵循“左物右码”的原则,结合配制溶质质量分数一定的溶液的基本步骤,进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为16%的氯化钠溶液,需氯化钠的质量=100g×16%=16g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-16g=84g(合84mL).
(2)图①中玻璃棒搅拌的目的是加快溶解速率.
(3)托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图③中所示操作错误.
配制100克溶质质量分数为16%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,配制溶液的正确操作顺序是⑤③④②①.
故答案为:(1)16;84;(2)加快溶解速率;(3)③;⑤③④②①.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
2.把100g溶质质量分数为10%的食盐溶液稀释成2%的食盐溶液,不需要用到的仪器是( )
| A. | 量筒 | B. | 烧杯 | C. | 玻璃棒 | D. | 托盘天平 |
19.下列说法正确的是( )
| A. | 家用电器着火时应立即用水浇灭 | |
| B. | 堆放杂物的纸箱着火用水浇灭,降低了可燃物的着火点 | |
| C. | 油锅着火时,可立即盖上锅盖灭火 | |
| D. | 为灭掉室内的大火,应立即打开门窗降温 |
6.分析推理是化学学习常用的方法,下列推理正确的是( )
| A. | 分子是构成物质的微粒,所以物质都是由分子构成的 | |
| B. | 燃烧需要同时具备是三条件,所以灭火只需要破坏其中一个即可 | |
| C. | CO和CO2组成元素相同,所以化学性质也相同 | |
| D. | 浓盐酸具有挥发性,所以浓硫酸也具有挥发性 |
16.成语”釜底抽薪“的本意包含着灭火的原理.下列灭火方法也依据这个原理的是( )
| A. | 消防队员用高压水枪灭火 | B. | 用液态二氧化碳灭火器灭火 | ||
| C. | 用锅盖盖灭着火的油锅 | D. | 砍掉树木形成隔离带 |
3.如图为某反应在同一容器中反应前后微粒示意图.下列说法不正确的是( )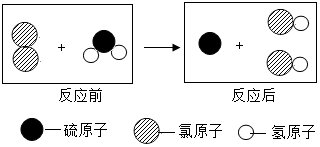

| A. | 化学反应前后分子保持不变 | B. | 该反应的化学式为Cl2+H2S=S+HCl | ||
| C. | 该反应为置换反应 | D. | 原子是化学变化中的最小粒子 |
20.下列物质的除杂实验中,所选用的试剂、方法及反应类型均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂、方法 | 反应类型 |
| A | CaCO3(CaO) | 高温 | 分解反应 |
| B | Fe(Fe2O3) | 足量CO | 置换反应 |
| C | CO2(CO) | 足量O2 | 化合反应 |
| D | CaCl2溶液(HCl) | 足量CaCO3 | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
18.下列有关物质构成的说法不正确的是( )
| A. | 物质可由分子、原子或离子构成 | |
| B. | 结构示意图为  、 、 的粒子,表示了同种元素的不同粒子 的粒子,表示了同种元素的不同粒子 | |
| C. | 相对原子质量为m的原子M,核外有n个电子,则核内中子数近似为:m-n | |
| D. |  所表示的原子,属于非金属元素原子 所表示的原子,属于非金属元素原子 |