题目内容
15. 鉴别碳酸钠溶液和氢氧化钠溶液的实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
鉴别碳酸钠溶液和氢氧化钠溶液的实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.(1)写出试管②中反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)【猜想】甲同学认为:只含氢氧化钠;
乙同学认为:只含碳酸钠;
丙同学认为:含有氢氧化钠和氢氧化钙;
丁同学认为:含有氢氧化钠、碳酸钠和氢氧化钙;
你认为还可能是含有氢氧化钠和碳酸钠(写一种猜想).
【讨论】你认为甲、乙、丙三位同学中那位同学的猜想不合理并叙述理由乙,滤液中一定含有氢氧化钠.
【实验设计】设计一个简单的实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,取滤液适量于试管中,滴加澄清石灰水 | 溶液变浑浊 | 你的猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入少量稀盐酸 | 无明显现象 | 猜想成立 |
【反思拓展】
下列实验方法可以区分氢氧化钠和氢氧化钙两种固体的是ACD(填字母).
A.放置在空气中 B.观察颜色 C.加水溶解 D.利用溶解性.
分析 碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
氢氧化钠和稀盐酸反应生成氯化钠和水,氢氧化钙和稀盐酸反应生成氯化钙和水;
氢氧化钠固体暴露在空气中容易潮解;
氢氧化钠易溶于水,氢氧化钙微溶于水.
解答 解:(1)试管②中,碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)【猜想】
如果碳酸钠过量时,滤液中的溶质是反应生成的氢氧化钠和过量的碳酸钠.
故填:含有氢氧化钠和碳酸钠.
【讨论】
乙的猜想不合理,这是因为滤液中一定含有碳酸钠和氢氧化钙反应生成的氢氧化钠.
故填:乙,滤液中一定含有氢氧化钠.
【实验设计】
实验过程如下表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,取滤液适量于试管中,滴加澄清石灰水 | 溶液变浑浊 | 你的猜想正确 |
甲同学对实验结果判断不正确,这是因为如果滤液中含有氢氧化钠和氢氧化钙时,滴加适量的稀盐酸时无明显现象.
故填:不正确,如果含有氢氧化钠和氢氧化钙时,滴加适量的稀盐酸时无明显现象.
【反思拓展】
A.放置在空气中时,表面出现潮湿的是氢氧化钠,无明显现象的是氢氧化钙,该选项可以区分两种物质;
B.氢氧化钠和氢氧化钙都是白色固体,通过观察颜色不能区分两种物质;
C.加水溶解时,如果水的量相同,溶解较多的是氢氧化钠,溶解较少的是氢氧化钙,该选项可以区分两种物质;
D.氢氧化钠和氢氧化钙的溶解能力不同,因此利用溶解性可以区分两种物质.
故填:ACD.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
6.实验室需配制一定浓度的硝酸钾溶液.
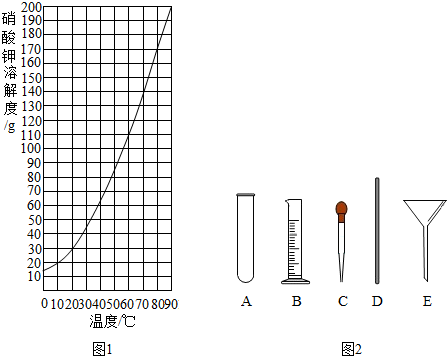
(1)查阅硝酸钾溶解性.由图可知,20℃时,硝酸钾的溶解度为31.6g,在该温度下配制硝酸钾溶液,溶质质量分数最大为24%(计算结果保留整数).
(2)计算.配制40g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为4g,所需蒸馏水的体积为36mL
(3)称量.分别在天平左右两盘放上纸片,调节平衡后,A(填字母).
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取.量取所需蒸馏水要用到的仪器是图2中的BC(填字母).
(5)溶解.将称量好的硝酸钾和蒸馏水混合溶解.
(6)稀释.20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出需要用到的数据:g/mL.
硝酸钾溶液的密度(单位g/mL)
(1)查阅硝酸钾溶解性.由图可知,20℃时,硝酸钾的溶解度为31.6g,在该温度下配制硝酸钾溶液,溶质质量分数最大为24%(计算结果保留整数).
(2)计算.配制40g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为4g,所需蒸馏水的体积为36mL
(3)称量.分别在天平左右两盘放上纸片,调节平衡后,A(填字母).
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取.量取所需蒸馏水要用到的仪器是图2中的BC(填字母).

(5)溶解.将称量好的硝酸钾和蒸馏水混合溶解.
(6)稀释.20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出需要用到的数据:g/mL.
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
20.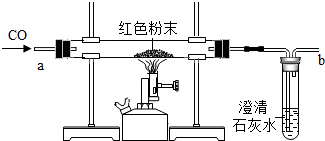 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
(1)【提出问题】假设l:红色粉末是铜粉;
假设2:红色粉末是氧化铁粉;
假设3:红色粉末是铜粉和氧化铁粉的混合物.
(2)【设计实验方案】同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如图所示).
请你完成下表:
(3)【进行实验】通过实验及分析,确认假设3成立.
(4)【反思与评价】
①实验过程中,硬质玻璃管内发生反应的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②实验时通入一氧化碳片刻后再加热的原因是防止加热一氧化碳和空气的混合气体时发生爆炸.
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是在b处用酒精灯点燃,或用塑料袋(气球)收集.
 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.(1)【提出问题】假设l:红色粉末是铜粉;
假设2:红色粉末是氧化铁粉;
假设3:红色粉末是铜粉和氧化铁粉的混合物.
(2)【设计实验方案】同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如图所示).
请你完成下表:
| 实验中可能出现的现象 | 结论 |
| 假设1成立 | |
| 假设2成立 | |
| 假设3成立 |
(4)【反思与评价】
①实验过程中,硬质玻璃管内发生反应的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②实验时通入一氧化碳片刻后再加热的原因是防止加热一氧化碳和空气的混合气体时发生爆炸.
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是在b处用酒精灯点燃,或用塑料袋(气球)收集.
7.学习了MnO2对过氧化氢分解有催化作用的知识后,小芳同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图实验:

(1)填写如表:
(2)步骤①的目的是证明不加氧化铜过氧化氢能产生氧气但是速率慢.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
(5)请你帮助小芳同学设计实验证明步骤⑤所得固体确实已经烘干,你的方案为:在固体上加无水硫酸铜,固体不变蓝,说明已经烘干.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图实验:

(1)填写如表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中产生气泡较快 带火星的木条复燃. | 固体质量不变 | 溶液中有气泡放出, 带火星的木条复燃 | 猜想成立. |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
(5)请你帮助小芳同学设计实验证明步骤⑤所得固体确实已经烘干,你的方案为:在固体上加无水硫酸铜,固体不变蓝,说明已经烘干.

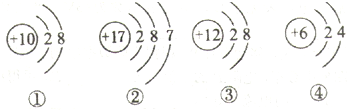
 已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如下图所示.
已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如下图所示. 如图是某同学鉴别碳酸氢铵、硫酸铵、硝酸铵三种化肥的过程(反应条件未标出),请回答下列问题:
如图是某同学鉴别碳酸氢铵、硫酸铵、硝酸铵三种化肥的过程(反应条件未标出),请回答下列问题: