题目内容
10.通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质.以下是制备精盐水的实验方案,各步操作流程如下: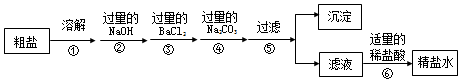
(1)写出沉淀中物质的化学式Mg(OH)2、BaSO4、CaCO3、BaCO3;
(2)步操④加入过量碳酸钠溶液的作用是除去氯化钙和过量的氯化钡;
(3)步操②中发生反应的化学方程式是MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
(4)步骤③与步骤④的顺序不能交换的原因是如果交换顺序,则无法除去过量的氯化钡.
分析 氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,和氯化钡反应生成碳酸钡沉淀和氯化钠;
稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳.
解答 解:(1)氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,和氯化钡反应生成碳酸钡沉淀和氯化钠,因此沉淀中物质的化学式是Mg(OH)2、BaSO4、CaCO3、BaCO3.
故填:Mg(OH)2、BaSO4、CaCO3、BaCO3.
(2)步操④加入过量碳酸钠溶液的作用是除去氯化钙和过量的氯化钡.
故填:除去氯化钙和过量的氯化钡.
(3)步操②中氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,发生反应的化学方程式是:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
故填:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(4)步骤③与步骤④的顺序不能交换的原因是:如果交换顺序,则无法除去过量的氯化钡.
故填:如果交换顺序,则无法除去过量的氯化钡.
点评 加入碳酸钠溶液、氢氧化钠溶液和氯化钡溶液除去杂质时,碳酸钠溶液应该在加入氯化钡溶液后再加入,否则过量的氯化钡溶液无法除去.

练习册系列答案
相关题目
6.对物质进行分类是化学学习的重要方法,下列物质按纯净物、碱、氧化物的顺序排列正确的是( )
| A. | 冰水混合物、纯碱、氯酸钾 | B. | 生铁、熟石灰、石油 | ||
| C. | 液氮、氢氧化钠、二氧化锰 | D. | 洁净的空气、碳酸钙、过氧化氢 |
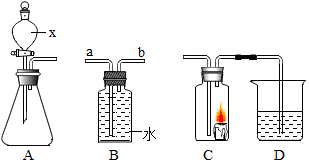
15.下列过程中不发生化学变化的是( )
| A. | 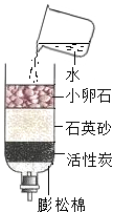 | B. |  | C. | 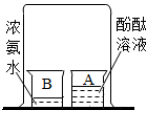 | D. |  |
2.常温下,实验室用过氧化氢制取氧气时,没有加催化剂,其结果是( )
| A. | 不影响化学反应速率 | B. | 反应速度慢.产生氧气的质量减少 | ||
| C. | 不产生氧气 | D. | 产生氧气的质量不变,反应速度慢 |
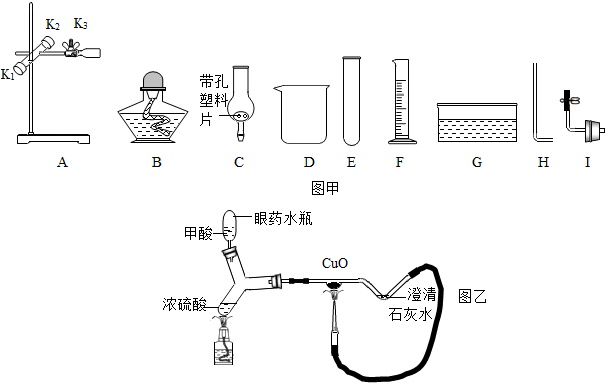
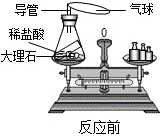 小明设计了一个实验来探究质量守恒定律.如图所示,反应前天平平衡,他取下此装置(装置气密性良好)将其倾斜,使稀盐酸(HCl)和大理石(主要成分是碳酸钙)接触,生成氯化钙、二氧化碳气体和水,待充分反应后,气球膨胀,再将装置放回天平左盘,此时他发现天平的指针向右偏转了.请回答下列问题:
小明设计了一个实验来探究质量守恒定律.如图所示,反应前天平平衡,他取下此装置(装置气密性良好)将其倾斜,使稀盐酸(HCl)和大理石(主要成分是碳酸钙)接触,生成氯化钙、二氧化碳气体和水,待充分反应后,气球膨胀,再将装置放回天平左盘,此时他发现天平的指针向右偏转了.请回答下列问题: 铝在工业和日常生活中应用广泛,请回答
铝在工业和日常生活中应用广泛,请回答