题目内容
实验室可用氯酸钾或过氧化氢制取氧气.
(1)过氧化氢的分解的变化可用下式表示:过氧化氢
水+氧气
上述变化所涉及的物质中,属于金属氧化物的是 ,氧元素的化合价为-1价的是 .
(2)用氯酸钾或过氧化氢制取氧气的实验中,都需要加入少量二氧化锰,二氧化锰的作用是 ;若未加入二氧化锰,则反应 (选填“不能发生”或“明显减慢”)
(3)若实验室用100g过氧化氢溶液,刚好制取了4.8g氧气,求该过氧化氢溶液的浓度.
(1)过氧化氢的分解的变化可用下式表示:过氧化氢
| 二氧化锰 |
上述变化所涉及的物质中,属于金属氧化物的是
(2)用氯酸钾或过氧化氢制取氧气的实验中,都需要加入少量二氧化锰,二氧化锰的作用是
(3)若实验室用100g过氧化氢溶液,刚好制取了4.8g氧气,求该过氧化氢溶液的浓度.
考点:实验室制取氧气的反应原理,有关溶质质量分数的简单计算,从组成上识别氧化物,有关元素化合价的计算,根据化学反应方程式的计算
专题:空气与水
分析:(1)根据氧化物的定义及金属氧化物的特点分析;根据化合物中化合价的代数和为0回答;
(2)根据催化剂的作用分析回答:改变化学反应的速率,而本身的质量和化学性质在反应前后都没有发生改变;
(3)根据化学方程式中氧气的质量计算过氧化氢的质量,并结合溶质的质量分数与过氧化氢溶液的质量计算溶液的浓度.
(2)根据催化剂的作用分析回答:改变化学反应的速率,而本身的质量和化学性质在反应前后都没有发生改变;
(3)根据化学方程式中氧气的质量计算过氧化氢的质量,并结合溶质的质量分数与过氧化氢溶液的质量计算溶液的浓度.
解答:解:(1)在过氧化氢的分解的变化过程中,涉及到的物质有:过氧化氢、二氧化锰、水和氧气,其中过氧化氢、二氧化锰和水都是由两种元素组成,且含有氧元素的化合物,即氧化物,但属于金属氧化物的是二氧化锰;这四种物质中都含有氧元素,其中氧气中氧元素的化合价为0,二氧化锰和水中氧元素的化合价都是-2,只有过氧化氢中氧元素的化合价是-1;
(2)用氯酸钾或过氧化氢制取氧气的实验中,都需要加入少量二氧化锰,二氧化锰在这儿作为催化剂,因此二氧化锰的作用是加快反应速率(或催化作用); 若未加入二氧化锰,则反应明显减慢,不会影响氧气的产量;
(3)设参加反应的过氧化氢的质量为x.
2H2O2
2H2O+O2↑
68 32
x 4.8g
=
x=10.2g
该过氧化氢溶液的浓度是:
×100%=10.2%
故答案为:(1)二氧化锰;过氧化氢;
(2)加快反应速率(或催化作用);明显减慢;
(3)答:该过氧化氢溶液的浓度是10.2%.
(2)用氯酸钾或过氧化氢制取氧气的实验中,都需要加入少量二氧化锰,二氧化锰在这儿作为催化剂,因此二氧化锰的作用是加快反应速率(或催化作用); 若未加入二氧化锰,则反应明显减慢,不会影响氧气的产量;
(3)设参加反应的过氧化氢的质量为x.
2H2O2
| ||
68 32
x 4.8g
| 68 |
| x |
| 32 |
| 4,8g |
x=10.2g
该过氧化氢溶液的浓度是:
| 10.2g |
| 100g |
故答案为:(1)二氧化锰;过氧化氢;
(2)加快反应速率(或催化作用);明显减慢;
(3)答:该过氧化氢溶液的浓度是10.2%.
点评:本题是有关氧气的两种不同的制取方法的探究,考查了物质的分类、元素的化合价、催化剂的作用、及有关方程式的计算,难度不大,依据已有的知识即可完成.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
下列实验现象正确的是( )
| A、铁丝在空气中燃烧,火星四射,生成黑色的固体 |
| B、打开盛浓盐酸的试剂瓶,在瓶口上方看到白烟 |
| C、欲称量锌粒与烧杯中稀盐酸反应前后的总质量,来验证质量守恒定律 |
| D、用导管向紫色石蕊试液中吹入呼出的气体,石蕊变红;加热溶液又变成紫色 |
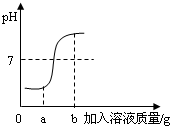 在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示:
在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示: ,Mg原子在化学反应中容易
,Mg原子在化学反应中容易