题目内容
12.为探究铁、锌、铜、铝、银五种金属的活动性顺序,进行如图所示的实验.(实验前金属片表面均打磨过)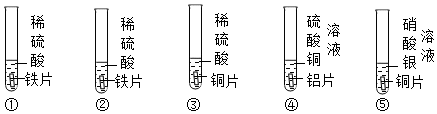
(1)实验④中反应的化学方程式为2Al+3CuSO4=Al2(SO4)3+3Cu.
(2)通过以上实验可以得出什么结论?
(3)为证明五种金属的活动性顺序,在以上实验的基础上需要补做实验,要求除金属单质外,只能再选一种试剂,写出实验操作、现象和结论.
分析 铝比锌活泼,锌比铁活泼,铁比铜活泼,铜比银活泼;
铝和硫酸铜反应生成硫酸铝和铜.
解答 解:(1)实验④中铝和硫酸铜反应生成硫酸铝和铜,反应的化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu.
故填:2Al+3CuSO4=Al2(SO4)3+3Cu.
(2)①中产生气泡,说明铁在金属活动性顺序中排在氢前面,②中产生气泡,说明锌在金属活动性顺序中排在氢前面,③中无明显现象,说明铜在金属活动性顺序中排在氢后面,④中铝片表面附着红色固体,说明铝比铜活泼,⑤中铜片表面附着银白色固体,说明铜比银活泼,因此可以得出什么结论是:铝、锌、铁比铜活泼,铜比银活泼.
故答案为:铝、锌、铁比铜活泼,铜比银活泼.
(3)实验方案是:取两支试管,分别加入适量硫酸锌溶液,其中1支试管中放入铁片,1支试管放入铝片,铁片表面无明显现象,说明锌比铁活泼,铝片表面附着银白色固体,说明铝比锌活泼.
故答案为:取两支试管,分别加入适量硫酸锌溶液,其中1支试管中放入铁片,1支试管放入铝片,铁片表面无明显现象,说明锌比铁活泼,铝片表面附着银白色固体,说明铝比锌活泼.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
2.某校化学兴趣小组的同学们帮助实验老师整理化学药品室时,发现两个未贴标签的试剂瓶中分别存放银白色金属片.到底它们是哪两种金属?请同学们设计实验方案对这两种金属X和Y的金属活动性顺序进行实验探究.
(1)进行实验,获得结论.完成好如下实验报告,并回答后续有关问题.
(2)在进行上述实验之前,实验老师只知道X、Y可能是铝、银中的各一种,则根据实验结果说明X是铝,反应的化学方程式为2Al+6HCl═2AlCl3+3H2↑.
(3)小明同学提出,还可以用其它方法证明X、Y的活动性.请你用化学方程式表示Al+3AgNO3═Al(NO3)3+3Ag(应有明显的实验现象).
(1)进行实验,获得结论.完成好如下实验报告,并回答后续有关问题.
| 实验步骤 | 实 验 现 象 | 结 论 |
| 分别把这两种金属放入稀盐酸 溶液中,观察. | 金属Y表面无明显变化;金属X的表面有大量气泡冒出.将燃着的木条放在金属X的试管口,气体燃烧. | 金属活动性顺序:X>Y |
(3)小明同学提出,还可以用其它方法证明X、Y的活动性.请你用化学方程式表示Al+3AgNO3═Al(NO3)3+3Ag(应有明显的实验现象).
20.下表是某研究性学习小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据.请你分析:该研究小组在设计方案时,考虑了浓度温度、催化剂、等因素对过氧化氢分解速率的影响.
用10mlH2O2溶液制取150mlO2所需的时间(秒):
用10mlH2O2溶液制取150mlO2所需的时间(秒):
| 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 |
| MnO2催化、不加热 | 10 | 25 | 60 |
7.课外小组的同学为探究锌、铜、镍三种金属的性质,进行如下实验.
【实验一】取一根铜丝,在铜丝一端滴上一滴石蜡,用酒精灯加热铜丝的另一端.
【实验二】取粗细、长短相同的锌丝、铜丝、镍(Ni)丝分别与50mL稀盐酸反应,
实验记录如表所示.
(1)实验一中观察到石蜡熔化,说明铜丝具有导热性.
(2)由实验二得出锌、铜、镍三种金属活动性由强到弱的顺序是锌、镍、铜.
【实验一】取一根铜丝,在铜丝一端滴上一滴石蜡,用酒精灯加热铜丝的另一端.
【实验二】取粗细、长短相同的锌丝、铜丝、镍(Ni)丝分别与50mL稀盐酸反应,
实验记录如表所示.
| 锌 | 镍 | 铜 | |
| 稀盐酸的质量分数 | 15% | 15% | 15% |
| 主要实验现象 | 大量气泡 | 少量气泡 | 无现象 |
(2)由实验二得出锌、铜、镍三种金属活动性由强到弱的顺序是锌、镍、铜.
4.关于 5%的食盐溶液,下列叙述正确的是( )
| A. | 100g水中溶有5g食盐 | B. | 5g食盐溶解在95g水中 | ||
| C. | 溶液中食盐和水的质量比为1:19 | D. | 食盐的溶解度为5g |
2.下列各组现象属于化学变化的一组是( )
| A. | 蜡烛燃烧、牛奶变酸 | B. | 干冰升华、煤气燃烧 | ||
| C. | 电灯发光、汽油挥发 | D. | 滴水成冰、形成酸雨 |
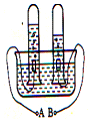 如图是电解水实验的示意图:
如图是电解水实验的示意图: