题目内容
工业用煅烧碳酸钙的方法制取二氧化碳.欲得到88吨二氧化碳,则需煅烧多少碳酸钙?同时得到氧化钙多少?
【答案】分析:煅烧碳酸钙生成氧化钙和二氧化碳,根据该反应的化学方程式确定反应中各物质的质量关系,由反应生成二氧化碳的质量计算碳酸钙及氧化钙的质量.
解答:解:设需煅烧碳酸钙的质量为x,同时得到氧化钙的质量为y
CaCO3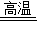 CaO+CO2↑
CaO+CO2↑
100 56 44
x y 88t
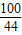 =
=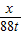 x=200t
x=200t
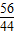 =
=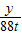 y=112t
y=112t
答:需煅烧200t碳酸钙,同时得到氧化钙112t.
点评:化学方程式可以表示反应中各物质的质量关系,利用反应中作任一物质的质量可计算出反应中其它物质的质量.
解答:解:设需煅烧碳酸钙的质量为x,同时得到氧化钙的质量为y
CaCO3
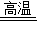 CaO+CO2↑
CaO+CO2↑100 56 44
x y 88t
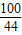 =
=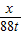 x=200t
x=200t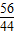 =
=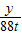 y=112t
y=112t答:需煅烧200t碳酸钙,同时得到氧化钙112t.
点评:化学方程式可以表示反应中各物质的质量关系,利用反应中作任一物质的质量可计算出反应中其它物质的质量.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
下列化学方程式符合题意且书写正确的是( )
| A、正常雨水的pH为5.6的原因CO2+H2O═H2CO3 | B、用盐酸除去铁器表面的铁锈FeO+2HCl═FeCl2+H2O | C、工业上用煅烧石灰石的方法制生石灰CaCO3═CaO+CO2 | D、证明铁的金属活动性比氢强2Fe+3H2SO3═Fe2(SO4)3+3H2↑ |