题目内容
13.下列的描述中正确的是( )| A. | 洁净新鲜的空气是一种纯净物 | B. | 空气中氮气的体积分数为21% | ||
| C. | 空气氧气的质量分数为21% | D. | 空气中氧气的体积分数为21% |
分析 从空气是由多种物质混合而成的,空气中各成分的体积分数去分析.
解答 解:A、洁净新鲜的空气也是由氧气、氮气等多种气体混合而成的,属于混合物,故错误;
B、空气中氮气的体积约占空气总体积的78%,故错误;
C、空气中氧气的体积分数为21%,不是质量分数,故错误;
D、空气中氧气的体积分数为21%,故正确;
故选:D
点评 记忆空气成分可以这样记忆:氧二一,氮七八,0.94是稀气,还有两个0.03,二氧化碳和杂气,并明确是体积分数而不是质量分数.

练习册系列答案
相关题目
3.铜片在空气中久置表面会变绿.某小组同学设计并进行实验,探究铜变绿的条件.
【查阅资料】1、铜绿的成分是碱式碳酸铜[Cu2(OH)2CO3],碱式碳酸铜能够与盐酸反应.
2、浓硫酸具有吸水性,可以作为一些气体的干燥剂.
【猜想与假设】常温下,铜片变绿可能与O2、CO2、水蒸气有关.
【进行实验】利用下图1装置分别制取并收集气体于试管中,制取气体原理及收集气体等操作见下表.将收集好的气体,用图2所示装置进行4个实验,通过控制与铜片接触的物质,进行实验并持续观察实验现象.

【解释与结论】
(1)实验1的目的是验证只与氧气和水接触,铜片不生锈.
(2)实验2制取气体反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)得出“铜片变绿一定与O2有关”的结论,依据的两个实验是2和3(填编号).
(4)实验4中,试管内的气体主要含有氧气和二氧化碳.
(5)上述实验可推知,铜片变绿的条件是O2、CO2、水蒸气同时存在.
【讨论与交流】
(6)同学们猜想碱式碳酸铜与盐酸反应有二氧化碳生成,证明此猜想所需试剂是澄清石灰水.
【查阅资料】1、铜绿的成分是碱式碳酸铜[Cu2(OH)2CO3],碱式碳酸铜能够与盐酸反应.
2、浓硫酸具有吸水性,可以作为一些气体的干燥剂.
【猜想与假设】常温下,铜片变绿可能与O2、CO2、水蒸气有关.
【进行实验】利用下图1装置分别制取并收集气体于试管中,制取气体原理及收集气体等操作见下表.将收集好的气体,用图2所示装置进行4个实验,通过控制与铜片接触的物质,进行实验并持续观察实验现象.

| 编号 | 主要实验操作 | 实验现象 |
| 1 | 甲中盛有过氧化氢溶液和二氧化锰,收集一试管气体 | 铜片始终无明显变化 |
| 2 | 甲中盛有大理石和稀盐酸,收集一试管气体 | 铜片始终无明显变化 |
| 3 | 甲处先用过氧化氢溶液和二氧化锰反应收集半试管气体,再换盛有大理石和稀盐酸的装置,继续收集至一试管气体 | 一段时间后铜片变绿 |
| 4 | 甲处先用过氧化氢溶液和二氧化锰反应收集半试管气体,再换盛有大理石和稀盐酸的装置,继续收集至一试管气体,并向气体中加入适量浓硫酸 | 铜片始终无明显变化 |
(1)实验1的目的是验证只与氧气和水接触,铜片不生锈.
(2)实验2制取气体反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)得出“铜片变绿一定与O2有关”的结论,依据的两个实验是2和3(填编号).
(4)实验4中,试管内的气体主要含有氧气和二氧化碳.
(5)上述实验可推知,铜片变绿的条件是O2、CO2、水蒸气同时存在.
【讨论与交流】
(6)同学们猜想碱式碳酸铜与盐酸反应有二氧化碳生成,证明此猜想所需试剂是澄清石灰水.
1.金的相对原子质量是197,质子数是79,则他的核电荷数是( )
| A. | 297 | B. | 118 | C. | 79 | D. | 197 |
5.下列描述物质化学性质的是( )
| A. | 食盐是白色固体 | B. | 铁球热胀冷缩 | ||
| C. | 二氧化碳使澄清石灰水变浑浊 | D. | 铝丝能折断 |
2.如图所示的化学实验基本操作中,正确的是( )
| A. | 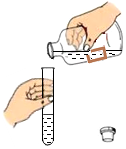 倾倒液体 | B. | 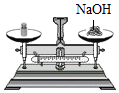 称量固体 | C. | 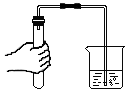 检验气密性 | D. | 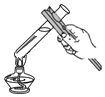 加热液体 |
