题目内容
1.有一种工业废水,其中含有大量的硫酸亚铁,少量的硫酸铜以及污泥.某同学设计了一个合理的方法回收铜和硫酸亚铁晶体.方案流程如图:
(1)步骤①中需采用是实验操作是过滤.
(2)固体X是铁和铜.
(3)步骤③中:需加入适量的物质是稀硫酸.
分析 过滤分离不溶性固体与液体,将废水中的污泥与溶液用过滤法分离,得溶液1中含有硫酸铜和硫酸亚铁,加入过量的铁将硫酸铜中的铜全部置换出来,过滤得到铜和铁的混合物和滤液硫酸亚铁,然后在固体混合物中加入适量硫酸与铁反应生成硫酸亚铁溶液,最后将硫酸亚铁溶液蒸发结晶即得硫酸亚铁晶体.
解答 解:(1)步骤①是将污泥与溶液分离,所以可用过滤;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,加入的铁是过量的,所以固体X是铁和铜;
(3)铁与硫酸铜反应生成铜和硫酸亚铁,因此经过步骤②之后得到的固体中含有生成的铜和剩余的铁,加入适量稀硫酸与铁反应生成硫酸亚铁,最后将溶液2和3合在一起进行蒸发结晶即可得到硫酸亚铁晶体.
故答案为:(1)过滤;
(2)铁和铜;
(3)稀硫酸.
点评 从废水中回收金属一般步骤先加入一种廉价金属置换出另一种金属,然后过滤,将过量金属除去即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列四种粒子的结构示意图中,最容易形成阳离子的是( )
| A. | 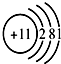 | B. | 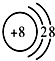 | C. | 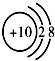 | D. | 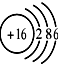 |
16.“催化转化器”可以将汽车尾气中有害气体处理为无污染的气体,如图为该反应的微观示意图,其中不同颜色的球代表不同的原子.下列说法正确的是( )
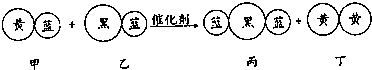
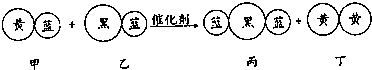
| A. | 乙和丙中所含的元素种类不同 | B. | 甲和丁中同种元素的化合价相等 | ||
| C. | 该反应中共有三种元素 | D. | 乙和丁都是化合物 |
6.下列现象不宜用质量守恒定律解释的是( )
| A. | 细铁丝在氧气中燃烧后固体质量增大 | |
| B. | 一氧化碳还原氧化铜后固体质量减小 | |
| C. | 高锰酸钾受热后剩余固体质量减小 | |
| D. | 水汽化变成质量相同的水蒸气 |
11.把O2,CO2,N2,Cl2关在一个房子里,(假设房子里无任何气体,且绝对密闭),然后打开房顶的烟囱,谁能够先全身而退( )
| A. | O2 | B. | CO2 | C. | N2 | D. | Cl2 |
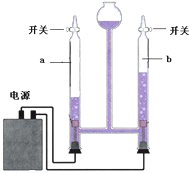 实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验.
实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验.