题目内容
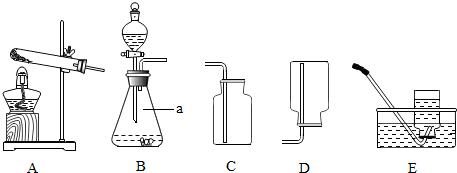
2. 某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.(1)烧瓶中观察到的现象是烧杯中的液体进入烧瓶,烧瓶中的液体变浑浊.
(2)根据上述现象,小静同学认为该现象无法证明氢氧化钠和二氧化碳发生了化学反应,理由是二氧化碳能够溶于水,能使澄清石灰水变浑浊.
(3)在排除上述可能后,兴趣小组又对实验结束后烧瓶内液体的溶质做出如下猜想:
猜想①:溶质只有氢氧化钠和碳酸钠;猜想②:溶质是氢氧化钠和氢氧化钙;
你还需补充的猜想③:溶质是氢氧化钠.
【设计实验】请设计实验方案验证你的猜想是正确的:
| 实验操作 | 实验现象 | 结论及反应的方程式 |
| 从烧瓶内取少量反应后的澄清溶液分别于两支试管中,分别滴加澄清石灰水、碳酸钠溶液 | 加入二者后均无明显现象 | 我的猜想正确 |
分析 (1)氢氧化钠能和二氧化碳反应生成碳酸钠和水,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
(2)二氧化碳能够溶于水,能使澄清石灰水变浑浊;
(3)根据反应物是否过量可以判断反应后溶液中含有溶质的情况.
解答 解:(1)二氧化碳和氢氧化钠反应后,烧瓶中的压强减小,在外界大气压作用下,烧杯中的澄清石灰水进入烧瓶中,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,因此烧瓶中观察到的现象是烧杯中的液体进入烧瓶,烧瓶中的液体变浑浊.
故填:烧杯中的液体进入烧瓶,烧瓶中的液体变浑浊.
(2)因为二氧化碳能够溶于水,能使澄清石灰水变浑浊,所以二氧化碳溶于氢氧化钠溶液后,烧瓶中的压强减小,在外界大气压作用下,烧杯中的澄清石灰水进入烧瓶中,二氧化碳能使澄清石灰水变浑浊,因此理由是二氧化碳能够溶于水,能使澄清石灰水变浑浊.
故填:二氧化碳能够溶于水,能使澄清石灰水变浑浊.
(3)猜想①:如果碳酸钠过量,溶质只有氢氧化钠和碳酸钠;猜想②:如果氢氧化钙过量,溶质是氢氧化钠和氢氧化钙;猜想③:如果恰好完全反应,溶质是氢氧化钠.
故填:氢氧化钠.
【设计实验】实验过程如下表所示:
| 实验操作 | 实验现象 | 结论及反应的方程式 |
| 从烧瓶内取少量反应后的澄清溶液分别于两支试管中,分别滴加澄清石灰水、碳酸钠溶液 | 加入二者后均无明显现象 | 我的猜想正确 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
12.小明同学对一种“汽泡爽”的冲调饮料进行了实验探究.
【饮料说明】
①主要原料:柠檬酸(C6H8O7)和小苏打(NaHCO3);
②使用说明:将一包“汽泡爽”粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料.
小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响.
【实验一】探究“汽泡爽”产生气体的成分.
(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3X↑,则X的化学式是CO2,为了检验该气体,小明应选择的试剂是澄清石灰水.
(2)如果实验室以柠檬酸和小苏打粉末混合后加水反应制取X气体,可以选择的发生装置是B(选填图1装置编号,下同),收集装置是C.
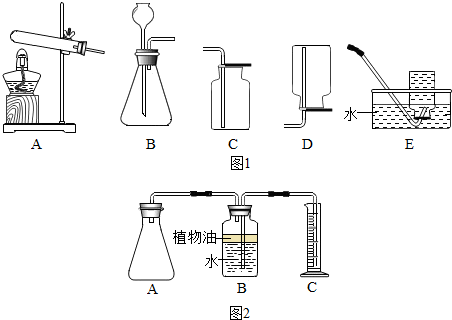
【实验二】探究加水温度对产生气体量的影响.
(1)小明先用冷水和热水各冲了一杯饮料,品尝时发现冷水冲的饮料中气泡较多,热水冲的饮料中气泡较少.他查阅资料发现:随着温度升高,气体在一定量的水中溶解的量会迅速降低.于是小明设计了如下对比实验方案,请填写表中空白.
(2)在老师的帮助下,小明采用相同的两套实验装置(如图2),编号为1、2,分别完成上述实验,在A中先加入水,再分别加入相同规格的一袋“汽泡爽”,迅速塞紧胶塞.量筒C用于收集A中产生的气体所排出的液体.B中油层的作用是防止二氧化碳溶解在B装置的水中.
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出,一包“汽泡爽”产生气体的量与反应物(柠檬酸和小苏打)的量有关,实验中小明所用的反应物量相等,产生气体的总量应该近似相等.请分析小明测得该组数据a、b相差较大的可能原因温度高气体在水中的溶解度小,收集到的气体多.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积.
【饮料说明】
①主要原料:柠檬酸(C6H8O7)和小苏打(NaHCO3);
②使用说明:将一包“汽泡爽”粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料.
小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响.
【实验一】探究“汽泡爽”产生气体的成分.
(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3X↑,则X的化学式是CO2,为了检验该气体,小明应选择的试剂是澄清石灰水.
(2)如果实验室以柠檬酸和小苏打粉末混合后加水反应制取X气体,可以选择的发生装置是B(选填图1装置编号,下同),收集装置是C.

【实验二】探究加水温度对产生气体量的影响.
(1)小明先用冷水和热水各冲了一杯饮料,品尝时发现冷水冲的饮料中气泡较多,热水冲的饮料中气泡较少.他查阅资料发现:随着温度升高,气体在一定量的水中溶解的量会迅速降低.于是小明设计了如下对比实验方案,请填写表中空白.
| 装置编号 | 加入水的体积 | 加入水的温度 | 收集到的气体的体积 |
| 1 | 200mL | 15℃ | a(待记录) |
| 2 | 200mL | 50℃ | b(待记录) |
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出,一包“汽泡爽”产生气体的量与反应物(柠檬酸和小苏打)的量有关,实验中小明所用的反应物量相等,产生气体的总量应该近似相等.请分析小明测得该组数据a、b相差较大的可能原因温度高气体在水中的溶解度小,收集到的气体多.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积.
10.关于Ca(OH)2叙述正确的是( )
| A. | 它的俗名叫生石灰,水溶液叫石灰水 | |
| B. | 它是一种白色粉末状固体,易溶于水 | |
| C. | 它的溶液能使紫色石蕊试液变成蓝色,使无色酚酞试液不变色 | |
| D. | 它能与碳酸钠溶液反应,来制备火碱 |
14.用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法.
[假设]小明的假设:澄清石灰水已变质. 小白的假设:气体X中除了有CO2外,还有HCl.
[实验探究](1)小明的探究:
(2)小白的探究
[实验反思]盐酸有很强的挥发性,用它制取气体往往不纯.
[假设]小明的假设:澄清石灰水已变质. 小白的假设:气体X中除了有CO2外,还有HCl.
[实验探究](1)小明的探究:
| 实验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用 澄清石灰 水是否变 质 | ①用一支试管另取少量原澄清石灰水 ②取稀硫酸与碳酸钠反应制取CO2 ③把二氧化碳通入澄清石灰水中 | 步骤③中现象为: 澄清石灰水变浑浊 | 步骤②中反应方程式为: Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ 实验结论:所用的澄清石灰水没有变质. |
| 实验目的 | 实验步骤 | 实验现象 | 化学方程式和实验结论 |
| 探究小白的假设是否成立 | 将气体X通入AgNO3溶液 | 产生白色沉淀 | 反应方程式为:HCl+AgNO3═AgCl↓+HNO3 实验结论:小白的假设成立 |
12.下列各组中溶液混合后,最终肯定有沉淀生成的是( )
| A. | Na2CO3、CaCl2、HCl | B. | Fe(NO3)2、H2SO4、HNO3 | ||
| C. | AgNO3、HNO3、HCl | D. | MgSO4、NaOH、HNO3 |
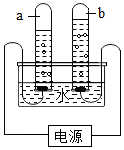 如图是电解水的简易装置.看图填空:
如图是电解水的简易装置.看图填空: