题目内容
化学与生活、生产息息相关,请用所学化学知识回答.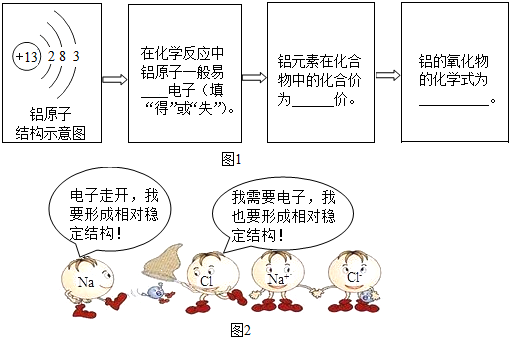
(1)H、C、O、Ca、Cl是初中常见的几种元素,请选用其中的元素写出符合下列要求的物质的化学式:
①人体胃液中含有的酸是 ; ②用作补钙剂的盐是 ;
③产生煤炉中蓝色火焰的物质是 ; ④最简单的有机化合物是 .
(2)从微观的角度认识物质及其变化,更有助于了解物质组成及变化的本质.
①填写图1:
已知:氧化铝是一种两性氧化物,既可以和酸反应又可以和碱反应,生成盐和水.请你写出氧化铝和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水的化学方程式 .
②如图2所示为氯化钠的形成过程,由此可推知:在形成氯化镁时,镁原子和氯原子的个数比为 .

(1)H、C、O、Ca、Cl是初中常见的几种元素,请选用其中的元素写出符合下列要求的物质的化学式:
①人体胃液中含有的酸是
③产生煤炉中蓝色火焰的物质是
(2)从微观的角度认识物质及其变化,更有助于了解物质组成及变化的本质.
①填写图1:
已知:氧化铝是一种两性氧化物,既可以和酸反应又可以和碱反应,生成盐和水.请你写出氧化铝和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水的化学方程式
②如图2所示为氯化钠的形成过程,由此可推知:在形成氯化镁时,镁原子和氯原子的个数比为
考点:化学式的书写及意义,原子和离子的相互转化,原子结构示意图与离子结构示意图,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:(1)人体胃液中的酸是盐酸,可以做补钙剂的是碳酸钙,煤炉中燃烧产生蓝色火焰的物质是一氧化碳,结构最简单的有机物是甲烷;
(2)①最外层电子数小于4的原子在发生反应时易失电子,而带正电,化合价为正价.化合价的数值是得失电子的数目;
②根据信息来书写化学方程式;
③根据最外层电子数来推断化合价,并书写化学式.
(2)①最外层电子数小于4的原子在发生反应时易失电子,而带正电,化合价为正价.化合价的数值是得失电子的数目;
②根据信息来书写化学方程式;
③根据最外层电子数来推断化合价,并书写化学式.
解答:解:(1)①盐酸是氯化氢气体的水溶液,其中氢元素显+1价,氯元素显-1价,故化学式为:HCl;
②在碳酸钙中,钙元素显+2价,碳酸根显-2价,故化学式为:CaCO3;
③在一氧化碳中,碳元素显+2价,氧元素显-2价,故化学式为:CO;
④甲烷的化学式为:CH4;
(2)①由铝原子结构示意图可知,最外层电子数是3小于4,在发生反应时易失电子,而带正电,化合价为+3价.氧通常显-2价,所以,铝的氧化物的化学式为 Al2O3;
②氧化铝和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O.
③在镁原子结构中,最外层有2个电子,易失去2个电子,氯原子最外层有7个电子,易得到1个电子,形成氯化镁时,镁原子和氯原子的个数比为:1:2.
故答案为:(1)①HCl;②CaCO3;③CO;④CH4;
(2)①失;+3;Al2O3;②Al2O3+2NaOH=2NaAlO2+H2O;③1:2.
②在碳酸钙中,钙元素显+2价,碳酸根显-2价,故化学式为:CaCO3;
③在一氧化碳中,碳元素显+2价,氧元素显-2价,故化学式为:CO;
④甲烷的化学式为:CH4;
(2)①由铝原子结构示意图可知,最外层电子数是3小于4,在发生反应时易失电子,而带正电,化合价为+3价.氧通常显-2价,所以,铝的氧化物的化学式为 Al2O3;
②氧化铝和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O.
③在镁原子结构中,最外层有2个电子,易失去2个电子,氯原子最外层有7个电子,易得到1个电子,形成氯化镁时,镁原子和氯原子的个数比为:1:2.
故答案为:(1)①HCl;②CaCO3;③CO;④CH4;
(2)①失;+3;Al2O3;②Al2O3+2NaOH=2NaAlO2+H2O;③1:2.
点评:考查了化学式的书写、化学方程式的书写以及原子结构的相关知识,难度适中.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
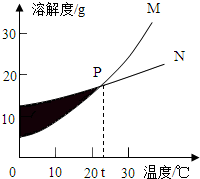 如图表示M、N两种固体物质的溶解度曲线,下列对图示信息的描述正确的是( )
如图表示M、N两种固体物质的溶解度曲线,下列对图示信息的描述正确的是( )| A、P点表示t℃时M、N的溶解度相等 |
| B、t℃时,M、N两种物质的溶液中溶质质量分数相等 |
| C、30℃时,M的饱和溶液中溶质的质量大于N饱和溶液 中溶质的质量 |
| D、阴影处各点对应的溶液(不包含曲线上的点)是M 的不饱和溶液,N的饱和溶液 |
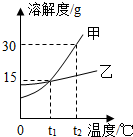 如图为甲、乙两物质的溶解度曲线,下列说法正确的是( )
如图为甲、乙两物质的溶解度曲线,下列说法正确的是( )| A、甲的溶解度大于乙的溶解度 |
| B、t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲=乙 |
| C、t1℃时,甲、乙两物质饱和溶液中所含溶质的质量相等 |
| D、t2℃时,将50克甲物质放入100克水中,得到溶液的质量为150克 |