题目内容
8.使燃料充分燃烧通常要考虑两点:一是燃烧时要有燃烧时要有足够多的空气,二是燃料有与它有足够大的接触面积.在日常生活中,燃料煤可以通过加工成煤粉和用鼓风机鼓入充足的空气的措施来达到以上两点从而使它充分燃烧.分析 从燃烧的条件分析,要使燃料充分燃烧可以增大氧气的浓度或与氧气的接触面积.
解答 解:使燃料充分燃烧可以从增大氧气的浓度或与氧气的接触面积来考虑.所以使燃料充分燃烧需考虑两点:一是燃烧时要有足够多的空气;二是燃料有与它有足够大的接触面积.在日常生活中,燃料煤可以通过将固体煤加工成煤粉和用鼓风机鼓入充足的空气的措施来达到以上两点从而使它充分燃烧.
故答案为:燃烧时要有足够多的空气;燃料有与它有足够大的接触面积;加工成煤粉;用鼓风机鼓入充足的空气.
点评 了解燃烧的条件,知道影响可燃物燃烧的因素是解答此题的关键.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案 精英口算卡系列答案
精英口算卡系列答案
相关题目
13.下列属于置换反应的是( )
①CaCO3+2HCl═CaCO3+CO2↑+H2O②Zn+2AgNO3═2Ag+Zn(NO3)2③Fe+H2SO4═FeSO4+H2↑④S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
①CaCO3+2HCl═CaCO3+CO2↑+H2O②Zn+2AgNO3═2Ag+Zn(NO3)2③Fe+H2SO4═FeSO4+H2↑④S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
20.在一定温度下,有一杯完全溶解的、饱和的氯化铵溶液,如果想把它变为不饱和溶液,下列可采 取的指施有(已知氯化铵固体的溶解度随温度的升高而增大)①降低温度②升高温度③加氯化铵固体④加溶剂⑤恒温蒸发溶剂( )
| A. | ①③④ | B. | ①③⑤ | C. | ②④ | D. | ②⑤ |
1.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验,向烧杯中的氢氧化钙溶液中滴加一定量的稀盐酸后,发现忘记滴加指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中溶质的成分进行研究.
(1)写出该反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O化学反应类型是复分解反应
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】A.溶质可能是CaCl2 和Ca(OH)2 B.溶质可能是CaCl2 C.溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想A,你认为排除猜想A的理由是氢氧化钙溶液显碱性,能使酚酞试液变红色
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
通过以上探究,最后确定猜想C正确.
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁质下水管道,可能造成的危害是腐蚀下水道,要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的碳酸钙,充分反应后过滤,反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(1)写出该反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O化学反应类型是复分解反应
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】A.溶质可能是CaCl2 和Ca(OH)2 B.溶质可能是CaCl2 C.溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想A,你认为排除猜想A的理由是氢氧化钙溶液显碱性,能使酚酞试液变红色
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液 | 若出现白色沉淀 | 则猜想B正确 |
| 若出现气泡,后出现白色沉淀 | 则猜想C正确 |
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁质下水管道,可能造成的危害是腐蚀下水道,要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的碳酸钙,充分反应后过滤,反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
2.下列实验或者操作方法能达到目的是( )
| 选项 | 要求 | 操作方法 |
| A | 检测溶液的酸碱度 | 加入酸碱指示剂,观察颜色变化 |
| B | 检测溶液是否为碱溶液 | 测定溶液的PH值 |
| C | 除去火碱溶液中的少量纯碱 | 加入适量氯化钡溶液,反应后过滤 |
| D | 除去水中的双氧水 | 适当加热或加入少量MnO2充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
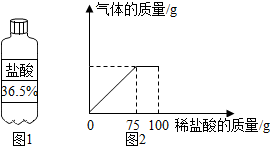 (1)配制溶质质量分数为7.3%的稀盐酸.
(1)配制溶质质量分数为7.3%的稀盐酸.