题目内容
6.请根据如图装置回答: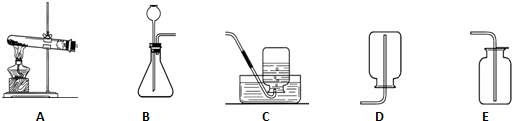
(1)在实验室可用同一气体发生装置制取O2、H2、CO2三种气体,写出用该装置制取O2的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)在实验室制取O2、H2、CO2三种气体的反应的共同点是CD(填序号).
A.需要加热 B.需用催化剂 C.没有气体参加反应 D.生成的气体只有一种
(3)实验室新进36%的浓盐酸,要把5g该浓盐酸稀释为5%的稀盐酸,需要水31克.配制该溶液时用到的玻璃仪器有:烧杯、玻璃棒和量筒和胶头滴管.
(4)化学上可通过多种反应得到NH3(NH3极易溶于水,密度比空气小),例如:
a.2NH4Cl(固)+Ca(OH)2(固)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
b.NH4HCO3(固)$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O
c.CaO(固)+NH3•H2O=NH3↑+Ca(OH)2
选用反应a在实验室制取NH3时,应选用图中的A(填装置序号)作为反应的发生装置;选用反应c在实验室制取NH3时,应选用上图中的B(填装置序号)作为反应的发生装置,实验室制取NH3不选择反应b的原因是有两种气体生成不易分离,收集NH3应选择装置D(填装置序号)
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
(2)实验室制取氧气、氢气、二氧化碳时,既有相同点,也有不同点;
(3)溶液稀释前后,溶质质量不变;
(4)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答 解:(1)在实验室可用B气体发生装置制取O2、H2、CO2三种气体,利用的药品分别是过氧化氢和二氧化锰、锌和稀硫酸、大理石或石灰石和稀盐酸,用该装置制取O2的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)在实验室制取O2、H2、CO2三种气体的反应的共同点是没有气体参加反应,生成的气体只有一种.
故填:CD.
(3)设需要水的质量为x,
根据题意有:5g×36%=(5g+x)×5%,
x=31g,
配制该溶液时用到的玻璃仪器有:烧杯、玻璃棒、量筒和胶头滴管.
故填:31;量筒和胶头滴管.
(4)选用反应a在实验室制取NH3时需要加热,应选用图中的A装置作为反应的发生装置;
选用反应c在实验室制取NH3时不需要加热,应选用上图中的B装置作为反应的发生装置;
实验室制取NH3不选择反应b的原因是有两种气体生成不易分离;
氨气极易溶于水,不能用排水法收集,密度比空气小,可以用向下排空气法收集,即用D装置收集.
故填:A;B;有两种气体生成不易分离;D.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 青少年缺钙易患夜盲症 | B. | 棉花属于合成材料 | ||
| C. | 硝酸钾属于钾肥 | D. | 多数维生素在人体内不能合成 |
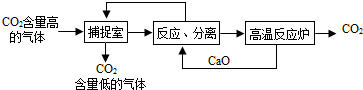
下列有关该方法的叙述中不正确的是( )
| A. | 能耗大是该方法的一大缺点 | |
| B. | 整个过程中,有两种物质可以循环利用 | |
| C. | “反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤 | |
| D. | 该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇(CH4O)等产品 |
| A. | 馒头和稀饭 | B. | 鸡蛋和牛奶 | C. | 油条和豆浆 | D. | 炸鸡块和酸奶 |