题目内容
1.自2008年6月1日起,我国禁止生产、销售、使用超薄塑料购物袋,并实行塑料购物袋有偿使用制度.这样做的主要目的是防止白色污染.新规定实行后预计塑料袋的使用量将减少$\frac{2}{3}$,但是其危害作用并没有根本解决,为尽量减少其危害,请你提出两条合理化建议用布袋代替塑料袋、使用可降解塑料等.日常生活中使用的塑料袋有两种,一种是用聚乙烯((CH2CH2)n]制成的,可用于盛装食品;另一种是用聚氯乙烯[(CH2CHCl)n]制成的.聚氯乙稀燃烧的化学方程式是:
(CH2CHCl)n+$\frac{5n}{2}$O2$\frac{\underline{\;点燃\;}}{\;}$2nCO2+nH2O+nHCl
(1)通过点燃的方法可以鉴别聚乙烯和聚氯乙烯.如果塑料点燃时有强烈的刺激性气味,这种塑料可能是由聚氯乙烯制成的.
(2)某同学设计了如图所示实验来验证塑料燃烧的产物.

若A瓶燃烧的是聚氯乙烯塑料,在B瓶中可以看到的现象是石蕊试纸变红,C、D两瓶中发生反应的化学方程式为HCl+AgNO3=AgCl↓+HNO3、CO2+Ca(OH)2=CaCO3↓+H2O.
若A瓶中用的是聚乙烯塑料,则在C瓶中不能(“能”或“不能’’)观察到沉淀.
分析 白色污染是人们对难降解的塑料垃圾(多指塑料袋)污染环境现象的一种形象称谓.它是指用聚苯乙烯、聚丙烯、聚氯乙烯等高分子化合物制成的各类生活塑料制品使用后被弃置成为固体废物,由于随意乱丢乱扔,难于降解处理,以致造成城市环境严重污染的现象;
(1)氯化氢气体是一种无色、辛辣的腐蚀性气体,具有令人窒息的臭味;它具有很强的水溶性.
(2)根据紫色石蕊试纸遇酸变红色,遇碱变蓝色;C瓶中是硝酸银,可与氯化氢反应生成氯化银白色沉淀和硝酸;D瓶中是氢氧化钙,可与二氧化碳反应,生成碳酸钙白色沉淀和水进行解答.
解答 解:因为白色污染是各类生活塑料制品使用后被弃置成为固体废物,由于随意乱丢乱扔,难于降解处理,以致造成城市环境严重污染的现象,故我国禁止生产、销售、使用超薄塑料购物袋,并实行塑料购物袋有偿使用制度.这样做的主要目的是防止白色污染;
为尽量减少其危害,我们可用布袋代替塑料袋,使用可降解塑料等;
(1)假如塑料点燃时有强烈的刺激性气味,则可能是氯化氢气体的气味,因为聚氯乙稀燃烧产生氯化氢气体,故这种塑料可能是由聚氯乙烯制成的;
(2)若A瓶燃烧的是聚氯乙烯塑料,产生HCl,紫色石蕊试纸遇酸变红色,故在B瓶中可以看到的现象是石蕊试纸变红;
C瓶中是氯化氢与硝酸银发生反应,化学方程式为:HCl+AgNO3=AgCl↓+HNO3;
D瓶中是氢氧化钙与二氧化碳反应,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
若A瓶中用的是聚乙烯塑料,不会生成氯化氢气体,所以在C瓶中不能观察到沉淀.
故答案为:防止白色污染;用布袋代替塑料袋;使用可降解塑料等;
(1)聚氯乙烯;
(2)石蕊试纸变红;HCl+AgNO3=AgCl↓+HNO3、CO2+Ca(OH)2=CaCO3↓+H2O;不能.
点评 本题主要考查学生对白色污染的概念和防止措施的掌握,由此可加强学生的环保意识.

| A. | 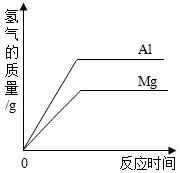 将等质量的镁和铝分别与足量的盐酸反应 | |
| B. | 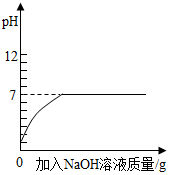 向pH=2的盐酸中滴加过量的氢氧化钠溶液 | |
| C. | 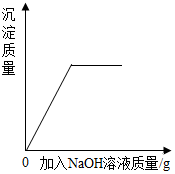 向盐酸和氯化铁的混合溶液中加入过量的氢氧化钠溶液 | |
| D. | 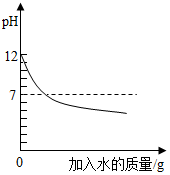 向pH=12的氢氧化钠溶液中加水稀释 |
| A. | HCl | B. | Cl2 | C. | Ca(ClO)2 | D. | KClO4 |
| A. | 氯吡苯脲由4种元素组成 | |
| B. | 它是一种氧化物 | |
| C. | 氯吡苯脲中元素质量比为12:10:1:30 | |
| D. | 它的相对分子质量为609.5 |
 程锦涛同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
程锦涛同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问: