题目内容
14.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | NaCl(Fe) | 适量的水 | 溶解、过滤、蒸发、结晶 |
| B | O2 (CO2) | 通过氢氧化钠溶液 | 洗气 |
| C | Ca(OH)2溶液 (NaOH) | 适量的纯碱溶液 | 过滤 |
| D | H2O(臭味) | 适量明矾 | 吸附 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、氯化钠易溶于水,Fe难溶于水,可采取加水溶解、过滤、蒸发、结晶的方法进行分离除杂,故选项所采取的方法正确.
B、CO2能与氢氧化钠溶液反应生成碳酸钠和水,O2不与氢氧化钠溶液反应,应再进行干燥,能除去杂质但引入了新的杂质水蒸气,不符合除杂原则,故选项所采取的方法错误.
C、Ca(OH)2溶液能与纯碱溶液反应生成碳酸钙沉淀和氢氧化钠,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、明矾溶于水生成的胶状物能对杂质进行吸附,但不能除去臭味,不能把杂质除去,不符合除杂原则,故选项所采取的方法错误.
故选:A.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
15. 如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )
 如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )| A. | 50℃时,A物质的溶解度最大 | |
| B. | 50℃时,把90gA物质放入100g水中能得到190g溶液 | |
| C. | 20℃时,B物质饱和溶液的溶质质量分数最大 | |
| D. | 升温可使C物质的不饱和溶液变成饱和溶液 |
2.工业生产的纯碱中常常含有一定量的氯化钠.为了测定某批次纯碱中碳酸钠的质量分数,小明同学称取12g纯碱样品放入烧杯中,用相同溶质质量分数的稀盐酸50g,分5次加入,每次充分反应后,称重、计算生成二氧化碳的质量,记录如下:
请回答:
(1)在第四次实验中,碳酸钠完全反应.
(2)求所取样品中碳酸钠的质量分数(计算结果保留一位小数).
| 实验次数 | 稀盐酸用量(g) | 生成二氧化碳的质量(g) |
| 1 | 10 | 1.1 |
| 2 | 10 | 2.2 |
| 3 | 10 | 3.3 |
| 4 | 10 | 4.4 |
| 5 | 10 | 4.4 |
(1)在第四次实验中,碳酸钠完全反应.
(2)求所取样品中碳酸钠的质量分数(计算结果保留一位小数).
9.下列关于碳和碳的氧化物的说法不正确的是( )
| A. | C和CO都可以将CuO中的Cu置换出来 | |
| B. | 在一定条件下CO2与CO可以相互转化 | |
| C. | 金刚石、石墨和C60都属于碳单质、但物理性质差异很大 | |
| D. | 温室效应既可以体现CO2的功,又可以体现CO2的过 |
19.化学是一门以实验为基础的科学,下面是我们在初中化学课中经历过的实验.
若按实验中发生的主要化学反应的基本反应类型进行分类,应将待分类组实验归为B组(填字母),你的分类依据是反应物与生成物均为一种单质和一种化合物.
| A组 | B组 | C组 | D组 | 待分类组 |
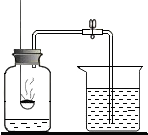 测定空气里氧气的含量 测定空气里氧气的含量 | 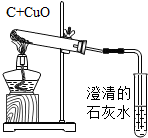 木炭还原氧化铜 木炭还原氧化铜 | 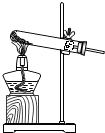 高锰酸钾制氧气 高锰酸钾制氧气 | 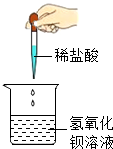 酸碱中和反应 酸碱中和反应 |  铁与硫酸铜溶液反应 铁与硫酸铜溶液反应 |
6.下列变化中,前者是化学变化,后者是物理变化的是( )
| A. | 轮胎爆炸、百炼成钢 | B. | 食物腐败、干冰升华 | ||
| C. | 钢铁生锈、庄稼长高 | D. | 工业制氧、石墨转化为金刚石 |
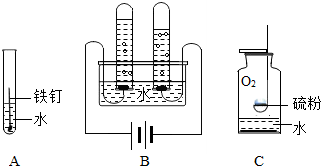 水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示回答下列问题:
水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示回答下列问题:
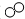 ”所代表的物质与单质铁发生化合反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,能观察到的现象是剧烈燃烧,火星四射,生成黑色固体.
”所代表的物质与单质铁发生化合反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,能观察到的现象是剧烈燃烧,火星四射,生成黑色固体.