题目内容
10.如图是一氧化碳还原氧化铜的装置.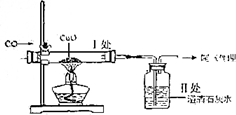
(1)实验开始时,先通入CO一会儿,再加热,其原因是防止一氧化碳和空气的混合气点燃,发生爆炸;
(2)指出实验中能证明一氧化碳还原氧化铜的证据是玻璃管中的黑色固体变成红色,澄清石灰水变浑浊;
(3)尾气处理装置通常是在导气管末端放一盏燃着的酒精灯,其作用是处理尾气,防止一氧化碳污染环境;
(4)若通入Ⅰ处的是CO和CO2的混合气体10g,且知该混合气体中含氧64%(Ⅰ处的CuO粉末和Ⅱ处的澄清石灰水均足量),则该混合气体中含CO的质量是5.6g;Ⅱ处最终生成的白色沉淀最有可能是C(填序号)
A.10g B.28g C.30g D.35g.
分析 (1)根据一氧化碳和氧气的混合气点燃,可能发生爆炸进行分析;
(2)根据一氧化碳和氧化铜在加热的条件下会生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊进行分析;
(3)根据一氧化碳有毒,需要尾气处理进行分析;
(4)根据混合气体氧元素的质量分数为64%及混合物的质量为10g,求出一氧化碳的质量;
根据碳元素守恒进行计算.
解答 解:(1)实验开始时,先通入CO一会儿,再加热,其原因是:防止一氧化碳和空气的混合气点燃,发生爆炸;
(2)一氧化碳和氧化铜在加热的条件下会生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以实验中能证明一氧化碳还原氧化铜的证据是:玻璃管中的黑色固体变成红色,澄清石灰水变浑浊;
(3)尾气处理装置通常是在导气管末端放一盏燃着的酒精灯,其作用是处理尾气,防止一氧化碳污染环境;
(4)设混合气体10g中一氧化碳的质量为x,则二氧化碳的质量为10g-x
$\frac{\frac{16}{28}×x+\frac{32}{44}×(10g-x)}{10g}$×100%=64%
x=5.6g
CO和CO2的混合气体10g,且知该混合气体中含氧64%,所以碳元素的质量为:10g×(1-64%)=3.6g
生成碳酸钙质量为:$\frac{3.6g}{12%}$=30g,故选:C.
故答案为:(1)防止一氧化碳和空气的混合气点燃,发生爆炸;
(2)玻璃管中的黑色固体变成红色,澄清石灰水变浑浊;
(3)处理尾气,防止一氧化碳污染环境;
(4)5.6g,C.
点评 本题主要考查了一氧化碳还原氧化铁的操作和注意事项,难度不大,需要在平时加强记忆.

练习册系列答案
相关题目
5.铜镁合金具有优良的导电性,常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
请回答下列问题并计算:
(1)表格中第三次实验时固体减少质量m=1.8g,铜镁合金中铜的质量分数为70%;
(2)反应结束后生成氢气的质量.(写出计算过程)
| 次 数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
| 固体减少质量/g | 1.8 | 1.8 | m | 0.6 |
(1)表格中第三次实验时固体减少质量m=1.8g,铜镁合金中铜的质量分数为70%;
(2)反应结束后生成氢气的质量.(写出计算过程)
15.有两种未知金属X和Y,其中Y能跟稀盐酸反应放出氢气;铜能把X从它的盐溶液中置换出来,则铜和两种未知金属活动性由强至弱的顺序是( )
| A. | X、Y、Cu | B. | Y、Cu、X | C. | Y、X、Cu | D. | X、Cu、Y |
20.下列有关实验现象的描述中不正确的是( )
| A. | 木炭在氧气中燃烧发出白光 | |
| B. | 细铁丝在氧气中剧烈燃烧,火星四射,生成一种白色物质 | |
| C. | 镁条在空气中燃烧发出耀眼的白光并放出大量的热 | |
| D. | 硫在空气中燃烧发出淡蓝色火焰,生成有刺激性气味的气体 |
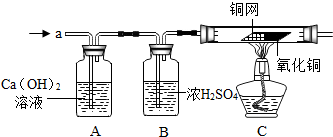 某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.生成的是什么气体呢?同学们决定进行探究.探究前老师提示,该反应生成的气体只有一种.
某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.生成的是什么气体呢?同学们决定进行探究.探究前老师提示,该反应生成的气体只有一种.