题目内容
9.看有元素的化合价在化学反应前后发生了变化,则该反应为氧化还原反应.据此可以判断下列化学反应属于氧化还原反应的是( )| A. | CaO+H2O═Ca(OH)2 | B. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | ||
| C. | CO2+NaOH═Na2CO3+H2O | D. | HCl+AgNO3═AgCl↓+HNO3 |
分析 由题目所给新信息:在化学反应前后有元素化合价变化的反应属于氧化还原反应,则可根据化合价的是否发生了变化判定哪些反应为氧化还原反应.
解答 解:A、在反应CaO+H2O═Ca(OH)2,各元素化合价均未出现变化,所以该反应不是氧化还原反应,故A错误;
B、2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,结合氢元素、氧元素的化合价可知,双氧水中氧元素的化合价为-1价,反应后变成氧气中的零价和水中的-2价,所以化学反应前后有化合价变化,属于氧化还原反应,故B正确;
C、在CO2+NaOH═Na2CO3+H2O中,反应前后化合价没有变化,不属于氧化还原反应,故C错误;
D、在HCl+AgNO3═AgCl↓+HNO3中,反应前后化合价没有变化,不属于氧化还原反应,故D错误.
故选B.
点评 本题难度不大,考查同学们的新信息获取、处理能力,充分理解氧化还原反应的含义是正确解题的关键.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
19.下列物质的用途中,应用到物质的化学性质的是( )
| A. | 将氦气充入气球中,使气球升到空中 | |
| B. | 利用干冰制造出舞台的烟雾效果 | |
| C. | 人们利用金属铜作为导线 | |
| D. | 人们利用煤气燃烧放出的热量煮饭、热水 |
4.如图是一定条件下某反应的微观模拟示意图,按图分析下列说法错误的是( )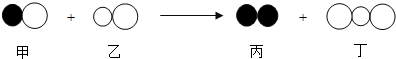

| A. | 反应前后,原子种类、数目不变 | |
| B. | 该反应中的甲、乙、丙、丁四种物质的分子个数比为2:2:1:2 | |
| C. | 该反应是化合反应 | |
| D. | 反应物和生成物都是由分子构成的 |
1.食品安全是公众普遍关注的问题,最近,“镉大米”成为公众关注的热点问题之一.据了解,含镉的大米对人的肝肾损害比较大.镉(Cd)的核电荷数为48,中子数为64,下列说法错误的是( )
| A. | 镉原子的质子数为48 | B. | 镉原子的相对原子质量为112g | ||
| C. | 镉是金属元素 | D. | 镉原子的核外电子数为48 |