题目内容
刘星表演了一组化学魔术:在A、B、C三个盛有无色液体的玻璃杯中,分别加入矿泉水瓶装的一种无色液体.同学们看到了奇特的现象:A杯变为“红葡萄酒”(变为红色);B杯变为“汽水”(产生大量气泡);C杯变为“牛奶”(出现白色浑浊).请你来揭开魔术的奥秘.
(1)矿泉水瓶中的液体是显碱性的盐溶液,则此盐溶液可能是 溶液;
(2)已知B杯中盛的是稀盐酸,则产生气体的用途之一是 ;
(3)若C杯中的药品是氯化钡溶液,则C中反应的化学方程式是 .
(1)矿泉水瓶中的液体是显碱性的盐溶液,则此盐溶液可能是
(2)已知B杯中盛的是稀盐酸,则产生气体的用途之一是
(3)若C杯中的药品是氯化钡溶液,则C中反应的化学方程式是
考点:物质的鉴别、推断,酸碱指示剂及其性质,酸的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见物质的推断题
分析:根据A、B、C三个玻璃杯中是无色液体,分别加入矿泉水瓶装的一种无色液体后,A杯中变成了红色,可能是碱性溶液与酚酞混合,B杯产生大量的气泡可能是碳酸盐与酸的反应,故可推测矿泉水瓶中可能盛的是碳酸钠,C杯中有白色沉淀,则可能是碳酸钠与氢氧化钙、氯化钙、氯化钡等生成沉淀的反应,然后将推出的各种物质代入转化关系中验证即可.
解答:解:(1)A、B、C三个玻璃杯中是无色液体,分别加入矿泉水瓶装的一种无色液体后,A杯中变成了红色,可能是碱性溶液与酚酞混合,B杯产生大量的气泡可能是碳酸盐与酸的反应,故可推测矿泉水瓶中可能盛的是碳酸钠,C杯中有白色沉淀,则可能是碳酸钠与氢氧化钙、氯化钙、氯化钡等生成沉淀的反应,碳酸钠溶液显碱性,可以使无色酚酞变红色,碳酸钠和盐酸反应会产生大量的气泡,碳酸钠和氢氧化钙、氯化钙、氯化钡等反应会生成白色沉淀,使溶液变浑浊,推导合理,矿泉水瓶中的液体是显碱性的盐溶液,则此盐溶液可能是Na2CO3;
(2)碳酸钠和盐酸反应会生成二氧化碳,二氧化碳具有密度比空气大,不助燃,不可燃的性质,可以用来灭火,产生气体的用途之一是:灭火;
(3)若C杯中的药品是氯化钡溶液,碳酸钠和氯化钡反应生成白色的碳酸钡沉淀和氯化钠,
化学方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl.
故答案为:(1)Na2CO3;
(2)灭火;
(3)BaCl2+Na2CO3=BaCO3↓+2NaCl.
(2)碳酸钠和盐酸反应会生成二氧化碳,二氧化碳具有密度比空气大,不助燃,不可燃的性质,可以用来灭火,产生气体的用途之一是:灭火;
(3)若C杯中的药品是氯化钡溶液,碳酸钠和氯化钡反应生成白色的碳酸钡沉淀和氯化钠,
化学方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl.
故答案为:(1)Na2CO3;
(2)灭火;
(3)BaCl2+Na2CO3=BaCO3↓+2NaCl.
点评:在解此类题时,首先分析题中的现象和物质之间的反应,然后依据学过的知识进行猜想,最后验证猜想的合理性,只要符合题意即可.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
某溶液的pH为4,要使这种溶液的pH升高到7,可采取的措施是( )
| A、加入适量的醋 |
| B、加入适量的洗衣粉 |
| C、加人大量的水 |
| D、通人大量二氧化碳气体 |
下列关于中和反应的叙述中,正确的是( )
| A、生成盐和水的反应就是中和反应 |
| B、中和反应一定是复分解反应 |
| C、中和反应中溶液的pH一定不变 |
| D、中和反应的生成物一定都是溶于水 |
下列反应属于复分解反应又属于中和反应的是( )
| A、CuO+2HCl=CuCl2+H2O |
| B、H2CO3=CO2↑+H2O |
| C、Ca(OH)2+H2SO4=CaSO4+2H2O |
| D、CO2+2NaOH=Na2CO3+H2O |
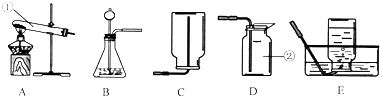
 九(2)班董军同学将浑浊的河水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用下图所示装置进行过滤,请问:
九(2)班董军同学将浑浊的河水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用下图所示装置进行过滤,请问: