题目内容
把50g 10%的氢氧化钠溶液和100g 20%的氢氧化钠溶液混合,求混合后溶液中溶质的质量分数?(写出必要的计算过程)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据溶质质量分数公式进行计算,找准溶质质量和溶液质量.
解答:解:混合溶液中溶质的质量分数为:
×100%≈16.7%
答案:所得溶液中溶质的质量分数是16.7%
| 50g×10%+100g×20% |
| 50g+100g |
答案:所得溶液中溶质的质量分数是16.7%
点评:本题考查了根据溶质质量分数进行的计算,完成此题,可以依据溶质质量分数公式进行.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
在①过滤:②溶解:③蒸发:④取液体试剂;⑤取固体试剂等实验操作中,一定要用玻璃棒的是( )
| A、①② | B、①②③ |
| C、①②③④⑤ | D、① |
下列对质量守恒定律的理解,正确的是( )
| A、因为“质量守恒”,所以煤燃烧后产生的煤渣质量一定和反应前煤的质量相等 |
| B、镁条在空气中燃烧后,生成物的质量比镁的质量大 |
| C、100g水与100g酒精混合后,质量等于200g,这符合质量守恒定律 |
| D、1g氢气在9g氧气中完全燃烧生成了10水 |
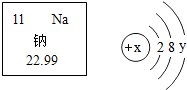 图示元素周期表中的一格和该元素的原子结构示意图,下列叙述不正确的是( )
图示元素周期表中的一格和该元素的原子结构示意图,下列叙述不正确的是( )| A、该元素为金属元素 |
| B、x值为11,y值为1 |
| C、该元素的相对原子质量为22.99 |
| D、该元素的原子失去电子形成离子,其离子符号为Na- |
 已知白磷的着火点为40°C,红磷的着火点为240°C.
已知白磷的着火点为40°C,红磷的着火点为240°C.