题目内容
 某研究性学习小组对“H2S的水溶液是否显酸性”进行探究.请你参与他们的探究活动,并回答有关问题.
某研究性学习小组对“H2S的水溶液是否显酸性”进行探究.请你参与他们的探究活动,并回答有关问题.【查阅资料】①H2S是一种无色、有臭鸡蛋气味的有毒气体,能溶于水.
②稀盐酸能使蓝色石蕊试纸变红色.
【提出假设】H2S的水溶液显酸性.
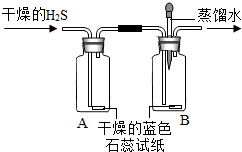
【实验探究】设计如图所示装置进行验证实验.
(1)实验过程中,A装置内蓝色石蕊试纸的颜色始终没有变化.A装置的作用是
(2)在通入H2S之前将B装置中胶头滴管内的蒸馏水滴到蓝色石蕊试纸上,未见试纸颜色发生变化,此操作的目的是
【结论】原假设成立.
【反思与评价】该验证实验中,有一个明显疏漏,请你指出疏漏之处为
【知识拓展】H2S的水溶液显酸性,具有酸的通性,若用氢氧化钠溶液吸收尾气,则反应的化学方程式为
考点:实验探究物质的性质或变化规律,碱的化学性质,溶液的酸碱性测定,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:本题探究了H2S的性质和变化规律,本题设计的实验步骤是①先把干燥的H2S通入干燥的蓝色石蕊试纸上,现象是不变色;②B装置中胶头滴管内的蒸馏水滴到蓝色石蕊试纸上,未见试纸颜色发生变化;再通入H2S气体,蓝色石蕊试纸变红色,由此得出结论,H2S溶于水呈酸性.还要注意H2S有毒,会污染空气;根据酸碱中和反应生成盐和水的过滤书写化学方程式.
解答:解:【实验探究】(1)A装置内蓝色石蕊试纸的颜色始终没有变化,说明干燥的H2S不能使蓝石蕊试纸变色.故填:证明H2S气体不能使蓝色石蕊试纸变色(或干燥的H2S不显酸性);
(2)在通入H2S之前将B装置中胶头滴管内的蒸馏水滴到蓝色石蕊试纸上,未见试纸颜色发生变化,说明水不能使其变色.当有H2S通过时发现润湿的蓝色石蕊试纸变红,说明H2S溶于水呈酸性.故填:证明水不能使蓝色石蕊试纸变色(或证明水无酸性); 硫化氢的水溶液显酸性;
【反思与评价】查阅资料可知:H2S有毒,会污染空气,因此对尾气要进行处理.故填:没有尾气处理(或吸收)装置;
【知识拓展】H2S的水溶液显酸性,具有酸的通性,若用氢氧化钠溶液吸收尾气会生成盐和水,反应的化学方程式为 2NaOH+H2S=Na2S+2H2O.故填:2NaOH+H2S=Na2S+2H2O.
(2)在通入H2S之前将B装置中胶头滴管内的蒸馏水滴到蓝色石蕊试纸上,未见试纸颜色发生变化,说明水不能使其变色.当有H2S通过时发现润湿的蓝色石蕊试纸变红,说明H2S溶于水呈酸性.故填:证明水不能使蓝色石蕊试纸变色(或证明水无酸性); 硫化氢的水溶液显酸性;
【反思与评价】查阅资料可知:H2S有毒,会污染空气,因此对尾气要进行处理.故填:没有尾气处理(或吸收)装置;
【知识拓展】H2S的水溶液显酸性,具有酸的通性,若用氢氧化钠溶液吸收尾气会生成盐和水,反应的化学方程式为 2NaOH+H2S=Na2S+2H2O.故填:2NaOH+H2S=Na2S+2H2O.
点评:本考点探究了硫化氢溶于水呈酸性,属于实验探究题,既有实验过程的探究,又有结论的探究.首先提出问题、查阅资料,然后设计实验方案、进行实验,最后得出正确的结论,这是探究题的一般步骤和思路.

练习册系列答案
相关题目
在一定条件下,氨气容易液化而成为液氨,液氨可以燃烧,其燃烧的化学方程式为:4NH3+3O2
2X+6H2O下列说法中正确的是( )
| ||
| A、液氨属于混合物 |
| B、NH3中N元素的化合价为-1 |
| C、X的化学式为NO |
| D、液氨具有可燃性,可用作燃料 |
蜡烛(足量)在如图1密闭装置内燃烧至熄灭,用仪器测出这一过程中瓶内氧气含量的变化如图2所示.下列判断正确的是( )


| A、蜡烛燃烧前装置内只有氧气 |
| B、氧气浓度小于一定值时,蜡烛无法燃烧 |
| C、过程中装置内物质总质量不断减少 |
| D、蜡烛熄灭后瓶内只剩二氧化碳气体和水蒸气 |
类推是常用的思维方法.以下类推正确的是( )
| A、分子可以构成物质,所以物质一定由分子构成 |
| B、单质只含一种元素,所以含一种元素的物质一定是单质 |
| C、有机物都含碳元素,所以含碳元素的化合物一定是有机物 |
| D、酸溶液的pH小于7,所以柠檬酸溶液的pH一定小于7 |
下列说法中正确的是( )
| A、由一种元素组成的物质一定是单质 |
| B、任何纯净物都是由一种元素组成的 |
| C、含有氧元素的化合一定是氧化物 |
| D、溶液呈碱性的不一定是碱的溶液 |
下列说法中正确的是( )
| A、常温下金属都是固体 |
| B、钠比铝抗腐蚀能力强 |
| C、青铜、生铁、焊锡均属合金 |
| D、铁锈能阻止铁继续锈蚀 |
