题目内容
某化合物的化学式是H2nRO2n+1,其式量是M,则R的相对原子质量是 .
分析:根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
解答:解:某化合物的化学式是H2nRO2n+1,其式量是M,设R的相对原子质量是x,则1×2n+x+16×(2n+1)=M,则x=M-34n-16.
故答案为:M-34n-16.
故答案为:M-34n-16.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某化合物中H、S两元素的化合价为+1、-2,该化合物的化学式是
A. | B. | C.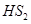 | D. |
(6分)下表是元素周期表的一部分:
|
族 周期 |
IA |
|
0 |
|||||
|
一 |
1 H 1.008 |
ⅡA |
ⅢA |
ⅣA |
V A |
ⅥA |
ⅦA |
2 He 4.003 |
|
二 |
3 Li 6.941 |
4 Be 9.012 |
5 B 10.81 |
6 C 12.01 |
7 N 14.01 |
8 O 16.00 |
9 F 19.00 |
10 Ne 20.18 |
|
三 |
11 Na 22.99 |
12 Mg 24.31 |
13 Al 26.98 |
14 Si 28.09 |
15 P 30.97 |
16 S 32.06 |
17 Cl 35.45 |
18 Ar 39.95 |
(1)Ne元素的原子核电荷数为_______,形成单质的化学式是 。
(2)某元素的原子结构示意图如右,则X的值为 。该元素与17号元素形成的化合物的化学式是 ,化合物中阴离子的结构示意图是 。

(3)请用表中的元素符号所组成的反应物写出符合要求的化学方程式:有水生成的化合反应:________________________________________。
 如图为某化合物的分子模型,该化合物是一种高效食品防腐剂.下列说法不正确的是( )
如图为某化合物的分子模型,该化合物是一种高效食品防腐剂.下列说法不正确的是( )