题目内容
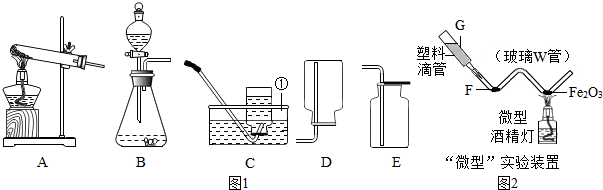
1.(1)人们使用天然气(主要成分为甲烷)过程中要注意通风,如果氧气不足会产生一氧化碳,使人中毒.某兴趣小组在实验室利用下列实验装置,在老师指导下制取氧气和甲烷,并检验甲烷燃烧后的气体产物.①小王用加热无水醋酸钠和碱石灰固体中的氢氧化钠反应生成甲烷,发生装置应选择图1中的A(填字母).

②小李用一定溶质质量分数的过氧化氢溶液和二氧化锰固体制取并收集一瓶干燥的氧气,请从图1选择装置图,正确的组装顺序为CFD(填字母),反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③下面是小张对甲烷在氧气中燃烧后的气体产物进行验证的实验.(图2)(假定每步均完全反应)请完成实验报告:

| 实验操作 | 实验现象 | 实验结论 |
| 将燃烧后气体产物进行验证 | 甲中的白色固体变蓝 | 燃烧产物中有H2O |
| 乙装置质量增加 | 燃烧产物中有CO2,乙瓶中反应方程式2NaOH+CO2═Na2CO3+H2O | |
| 丁中玻璃管内固体红色变成黑色、戊中石灰水变浑浊 | 燃烧产物中有CO,丁中玻璃管内反应方程式 Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
[提出问题]如何鉴别两种无色溶液?
[实验方案]小林等几位同学进行了如图3所示的实验.请你回答下列问题:
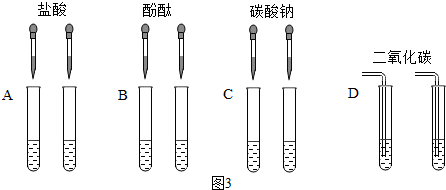
①C组实验中反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
②其中不能达到实验目的是A、B(填字母);
③D组实验中变浑浊的原溶液是澄清石灰水或Ca(OH)2溶液.
[继续探究]实验结束后,小林同学将A、B、C、D四组试管中的物质全部倒入同一个干净的烧杯中,充分反应后,得到无色澄清透明的溶液,对该溶液的成分又进行了探究.
[提出问题]该溶液中除水、酚酞外还含有哪些物质?
[查阅资料]氯化钙溶液呈中性.
[猜想与假设]Ⅰ.NaCl、CaCl2Ⅱ.NaCl、CaCl2Ⅲ.NaCl、CaCl2、NaOH
[反思与拓展]上述猜想与假设中只有一个不成立,它是Ⅲ(填序号).
分析 (1)制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气可以用浓硫酸干燥,收集干燥的氧气必须用向上排空气法收集,不能用排水法.用无水醋酸钠(化学式为CH3COONa)和碱石灰固体混合加热制取甲烷,因此需要加热;醋酸钠与氢氧化钠反应生成甲烷和碳酸钠.由题目的信息可知:无水硫酸铜吸水后变蓝,常用于吸收水和验证水的存在,因此甲装置是检验水的,乙装置质量增加说明有二氧化碳生成,如果将甲、乙装置顺序进行交换,则不能验证燃烧产物中有水生成,因为氢氧化钠溶液中有水;丁中玻璃管内固体颜色变化是红色变成黑色,戊中澄清石灰水变浑浊,说明生成了铁和二氧化碳,即一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;
(2)【实验方案】①根据碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠来分析;
②根据反应的现象进行鉴别;
③根据二氧化碳和氢氧化钙反应产生碳酸钙沉淀分析;
【猜想与假设】根据反应的程度分析溶质的成分;
【反思与拓展】根据现象得到无色澄清透明的溶液分析猜想的合理性
解答 解:(1)①用无水醋酸钠(化学式为CH3COONa)和碱石灰固体混合加热制取甲烷,因此需要加热;醋酸钠与氢氧化钠反应生成甲烷和碳酸钠;故答案为:A;
②如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气可以用浓硫酸干燥,收集干燥的氧气必须用向上排空气法收集;故答案为:CFD;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③已知“燃烧产物中有CO2”,乙瓶中为氢氧化钠溶液,故反应化学方程式为2NaOH+CO2═Na2CO3+H2O;而“丁中玻璃管内固体红色变成黑色、戊中石灰水变浑浊”,则说明气体产物中有一氧化碳,故丁中玻璃管内反应方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)【实验方案】①碳酸钠和氢氧化钙反应生成白色的碳酸钙沉淀和氢氧化钠,反应的现象为:生成白色沉淀;其化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
②A方案都反应,但都无现象,故不能鉴别;B方案都变成红色,故不能鉴别;而C和D都能出现不同的现象,因此不能达到实验目的是A、B;
③二氧化碳和氢氧化钙反应产生碳酸钙沉淀,而和氢氧化钠反应物现象,故D组实验中变浑浊的原溶液是石灰水;
【猜想与假设】若恰好完全反应,则只含有反应产生的氯化钠和氯化钙;
【反思与拓展】Ⅲ的猜想中含有氢氧化钠,能够使酚酞试液变成红色,而现象得到无色澄清透明的溶液,因此Ⅲ不合理;
故答案为:
(1)①A.
②CFD,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.③
| 实验操作 | 实验现象 | 实验结论 |
| 将燃烧后气体产物进行验证 | ||
| 2NaOH+CO2═Na2CO3+H2O | ||
| Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
[猜想与假设]NaCl、CaCl2;[反思与拓展]Ⅲ
点评 本考点主要考查了气体的制取装置和收集装置的选择、气体的干燥,同时也考查了化学方程式的书写等,综合性比较强;还考查了常见物质的鉴别,在做此类题时,首先弄清所要鉴别的物质的不同性质,然后选择适当的试剂进行鉴别,出现不同的现象,在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物的过量问题.

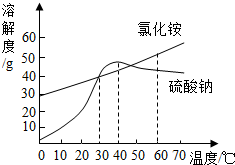 如图是氯化铵和硫酸钠的溶解度曲线示意图,由此得到的结论正确的是( )
如图是氯化铵和硫酸钠的溶解度曲线示意图,由此得到的结论正确的是( )| A. | 只有在 30℃时,两种物质的溶解度才相等 | |
| B. | 硫酸钠的溶解度随温度升高而增大 | |
| C. | 40℃时硫酸钠饱和溶液比氯化铵饱和溶液溶质质量分数大 | |
| D. | 40℃时,将硫酸钠溶液的温度升高,有晶体析出 |
| A. | “低碳经济”的含义是节约能源,减少二氧化碳的排放,控制“温室效应” | |
| B. | 羊毛和棉花属于天然纤维 | |
| C. | “白色污染”可以通过一些新型的、可降解的塑料加以控制 | |
| D. | “绿色食品”是不含任何化学物质的食品 |
| A. | +3 | B. | +1 | C. | +5 | D. | -3 |
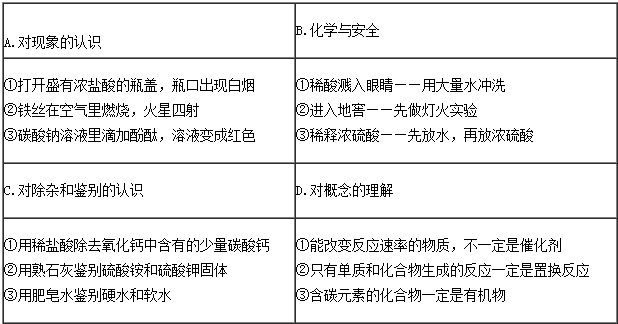
| A. | A | B. | B | C. | C | D. | D |
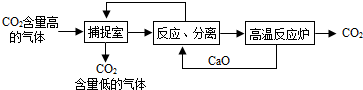
该实验小组同学通过查阅资料,进行了尝试.

【阅读资料】
不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.右表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
(2)实验中,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式2HCl+CuO=CuCl2+H2O;你认为步骤b调节溶液的pH到3.2-4.7(填数值范围)比较合适.
(3)实验中,步骤d加稀盐酸前,因缺少洗涤(填操作名称)而使获得的氯化铁溶液不纯.
(4)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用C(用字母表示)最合理.
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸.
| A. |  熄灭酒精灯 | B. | 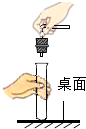 塞紧橡皮塞 | ||
| C. | 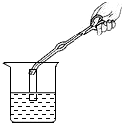 测定溶液的pH | D. | 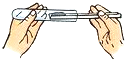 将固体粉末装入试管 |