题目内容
Mg某石灰石样品与足量稀盐酸反应(杂质不反应),共生成0.1mol二氧化碳.请计算:
①参加反应的碳酸钙的质量.(请根据化学方程式列式计算)
②已知该样品中含碳酸钙80%,则M= g.
【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算;有关化学方程式的计算.
【分析】由生成二氧化碳气体的质量,根据反应的化学方程式计算出石灰石中碳酸钙的质量,进而可计算出石灰石中的质量.
【解答】解:①0.1mol二氧化碳的质量为:0.1mol×44g/mol=4.4g
设需要碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
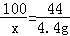
x=10g
②该样品中含碳酸钙80%,则M=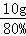 =12.5g
=12.5g
答案:
①参加反应的碳酸钙的质量为10g;
②12.5.
【点评】本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
 2MgO+C中作还原剂的物质是( )
2MgO+C中作还原剂的物质是( ) 是一门自然科学,研究和发展化学科学的基础是( )
是一门自然科学,研究和发展化学科学的基础是( ) CO2 4P+5O2
CO2 4P+5O2