题目内容
13.镁将成为21世纪重要的轻型环保材料,我国海洋中含有非常丰富的镁资源.从海水中提取镁的流程如下:海水中的氯化镁$→_{过滤}^{加熟石灰}$氢氧化镁$→_{蒸发结晶}^{盐酸}$MgCl2$\stackrel{通电}{→}$Mg
(1)整个流程中共涉及2个基本反应类型.写出上述流程中由氯化镁得到金属镁的化学方程式.
(2)金属镁是一种比较活泼的金属.如镁在二氧化碳中能燃烧生成氧化镁和一种黑色固体单质.
①若用金属镁测定空气中氧气的含量,所得结果和实际值相比偏大(选填“偏大”“偏小”或“不变”).
②根据上述信息我们对燃烧条件有了哪些新的认识(写出一条即可).
(3)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
猜想:①可能是氧化镁;②可能是Mg2(OH)2CO3,③可能是氢氧化镁.
根据已有知识小赵认为猜想①是错误的,其理由是因为氧化镁通常为白色固体.
实验探究:小赵对灰黑色物质进行加热,发现试管口有无色液滴出现,产生使澄清石 灰水变浑浊的气体,同时试管内生成白色固体.
实验分析:实验后,小赵认为③的猜测也是错误的,其理由是石灰水变浑浊的现象可说明此变化过程中有二氧化碳生成,而氢氧化镁中根本不含碳元素.
査阅资料得出结论:Mg2(OH)2CO3可以加热分解,产物均为氧化物,据此请你写出 Mg2(OH)2CO3分解的化学方程式Mg2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+H2O+CO2↑.
(4)某同学用部分被氧化的镁条10g放在足量的稀硫酸中充分反应后,共收集到0.6g 的氢气,请计算出该镁条中氧化镁的质量分数(假设镁只与氧气反应).
分析 (1)根据反应过程并结合反应类型的知识进行分析;
(2)根据测定空气中氧气的含量的原理及镁的性质分析.镁不仅与氧气反应,还能与氮气反应;
(3)猜想:根据物质颜色对猜想进行判断;
实验分析:根据探究实验结果,对猜想进行判断;
查阅资料得出结论:根据反应的特点,分析反应的生成物,完成反应化学方程式的书写;
(4)根据镁与H2SO4反应的化学方程式和生成氢气的质量,计算出参与反应的镁的质量,而得到氧化镁的质量,最后求出镁条中氧化镁的质量分数.
解答 解:(1)由制备流程可知,氯化镁和氢氧化钙反应、氢氧化镁和盐酸反应都属于复分解反应;氯化镁晶体失去结晶水、MgCl2通电会生成镁和氯气都属于分解反应;由氯化镁得到金属镁的化学方程式:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
故填:2;MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
(2)①在测定空气中氧气体积分数时用的可燃物只能与氧气反应,不能与空气中其它成分反应.镁不仅能与氧气反应还能与氮气反应,这样会导致水面上升超过$\frac{1}{5}$,结果偏大;
故填:偏大;
②有以上可知,燃烧不一定需要氧气;
(3)猜想:氧化镁通常为白色固体与镁表面呈灰色的现实不相符,因此猜想不成立;
故答案为:因为氧化镁通常为白色固体;
实验分析:实验中观察到澄清石灰水变浑浊,说明灰黑色物质分解出二氧化碳气体,则物质中含有C元素,而猜想的氢氧化镁在组成元素上不含C元素,因此猜想不成立;故故答案为:石灰水变浑浊的现象可说明此变化过程中有二氧化碳生成,而氢氧化镁中根本不含碳元素;
查阅资料得出结论:Mg2(OH)2CO3加热分解的产生均为氧化物,则分解生成MgO、H2O、CO2三种物质;
故答案为:Mg2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+H2O+CO2↑;
(4)设镁的质量为x
Mg+2HCl═MgCl2+H2↑
24 2
x 0.6g
$\frac{24}{2}=\frac{x}{0.6g}$
x=7.2g
镁条中氧化镁的质量分数为:$\frac{10g-7.2g}{10g}×100%$=28%
答:镁条中氧化镁的质量分数为28%.
点评 本题考查了基本反应类型的判断、根据化学方程式的有关计算以及明确物质之间的反应是解本题关键,题目难度较大.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 水果和蔬菜 | B. | 鸡蛋和肉 | C. | 花生油和奶油 | D. | 馒头和稀饭 |
| A. | 104.5g | B. | 104.8g | C. | 104.4g | D. | 104.7g |
| A. | 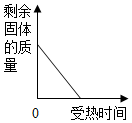 高温煅烧石灰石 | |
| B. | 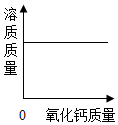 向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体 | |
| C. | 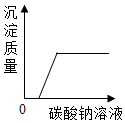 向盐酸和氯化钙的混合溶液中加入碳酸钠溶液 | |
| D. | 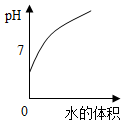 向pH=1的酸溶液中不断加水 |
| A. | 青蒿素由C、H、O三种元素组成 | |
| B. | 青蒿素中C、H、O三种元素的质量比为15:22:5 | |
| C. | 青蒿素的相对分子质量为282 | |
| D. | 一个青蒿素分子有42个原子构成 |
| A. | 涤纶和羊毛可以通过灼烧方法鉴别 | B. | 任何塑料袋都可以长期盛放食品 | ||
| C. | 橡胶都是人工合成材料 | D. | 合金、塑料、橡胶都属于合成材料 |
 化学是以实验为基础的科学,根据下面的实验回答问题:该实验的实验目的是验证质量守恒定律,该实验不能获得成功的原因是铁与稀硫酸反应生成硫酸亚铁和氢气,装置没有密封,生成的氢气逸出,图中所示称量的质量是73.2g.
化学是以实验为基础的科学,根据下面的实验回答问题:该实验的实验目的是验证质量守恒定律,该实验不能获得成功的原因是铁与稀硫酸反应生成硫酸亚铁和氢气,装置没有密封,生成的氢气逸出,图中所示称量的质量是73.2g.