题目内容
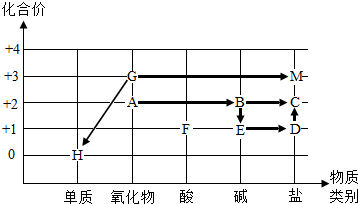 同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).
同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).请回答下列问题:
(1)工业上可用化合反应来制备B,且反应时放出大量热,B的俗称为
(2)E的固体露置在空气中一段时间后质量会增加,其原因是
(3)H、G均可与F溶液反应,分别生成含该金属元素的两种盐溶液,则G与F溶液反应的化学方程式为
(4)在B溶液中加入一定量D溶液,过滤后取滤液,滴入过量F溶液,无明显现象,则滤液中的溶质是(写出所有可能)
(5)已知金属铝可与E溶液反应生成偏铝酸钠(NaAlO2)和一种最轻的气体,写出该反应的化学方程式
考点:物质的鉴别、推断
专题:框图型推断题
分析:(1)根据生石灰溶于水放热分析;
(2)根据氢氧化钠吸水性和与二氧化碳反应分析;
(3)根据铁有亚铁盐和铁盐分析;
(4)根据氢氧化钠与氢氧化钙的化学性质分析;
(5)根据反应物、生成物结合质量守恒定律及书写方程式的原则书写方程式.
(2)根据氢氧化钠吸水性和与二氧化碳反应分析;
(3)根据铁有亚铁盐和铁盐分析;
(4)根据氢氧化钠与氢氧化钙的化学性质分析;
(5)根据反应物、生成物结合质量守恒定律及书写方程式的原则书写方程式.
解答:解:(1)工业上可用化合反应来制备B,B是一种碱,且反应时放出大量热,在学过的物质中氧化钙与水化合生成氢氧化钙,放出大量的热,因此B为熟石灰或消石灰,A为氧化钙;
(2)E是一种碱,露置在空气中一段时间后质量会增加,因此E是氢氧化钠,因其在空气中会吸水潮解,与二氧化碳反应生成碳酸钠而变质,故质量增加;
(3)F是一种酸,H是单质,G是氧化物,H、G都与酸反应生成含该金属元素的两种盐溶液,已知的元素中铁有+2和+3价,对应的盐有亚铁盐和铁盐,因此H是铁,G是氧化铁,G与F反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O或Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(4)B为氢氧化钙,在B溶液中加入D溶液产生沉淀,且D由氢氧化钠反应制取,因此D为碳酸钠,氢氧化钙与碳酸钠反应产生碳酸钙沉淀和氢氧化钠,过滤后取滤液,滴入过量的F(盐酸或硫酸)溶液无明显现象,说明碳酸钠没有剩余,氢氧化钙可能剩余,因此滤液中的溶质可能是氢氧化钠或氢氧化钠和氢氧化钙;
(5)金属铝可与E(氢氧化钠)溶液反应生成偏铝酸钠(NaAlO2)和一种最轻的气体(氢气)化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
故答案为:(1)熟石灰或消石灰;
(2)吸水潮解,与二氧化碳反应变质;
(3)Fe2O3+6HCl=2FeCl3+3H2O或Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(4)NaOH或NaOH和Ca(OH)2;
(5)2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(6)7故答案为:(1)熟石灰或消石灰 (2)吸收空气中的水分和二氧化碳
(3)Fe2O3+6HCl═2FeCl3+3H2O (4)①NaOH ②NaOH Ca(OH)2
(5)2Al+2NaOH+2H2O═2NaAlO2+3H2↑
(2)E是一种碱,露置在空气中一段时间后质量会增加,因此E是氢氧化钠,因其在空气中会吸水潮解,与二氧化碳反应生成碳酸钠而变质,故质量增加;
(3)F是一种酸,H是单质,G是氧化物,H、G都与酸反应生成含该金属元素的两种盐溶液,已知的元素中铁有+2和+3价,对应的盐有亚铁盐和铁盐,因此H是铁,G是氧化铁,G与F反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O或Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(4)B为氢氧化钙,在B溶液中加入D溶液产生沉淀,且D由氢氧化钠反应制取,因此D为碳酸钠,氢氧化钙与碳酸钠反应产生碳酸钙沉淀和氢氧化钠,过滤后取滤液,滴入过量的F(盐酸或硫酸)溶液无明显现象,说明碳酸钠没有剩余,氢氧化钙可能剩余,因此滤液中的溶质可能是氢氧化钠或氢氧化钠和氢氧化钙;
(5)金属铝可与E(氢氧化钠)溶液反应生成偏铝酸钠(NaAlO2)和一种最轻的气体(氢气)化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
故答案为:(1)熟石灰或消石灰;
(2)吸水潮解,与二氧化碳反应变质;
(3)Fe2O3+6HCl=2FeCl3+3H2O或Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(4)NaOH或NaOH和Ca(OH)2;
(5)2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(6)7故答案为:(1)熟石灰或消石灰 (2)吸收空气中的水分和二氧化碳
(3)Fe2O3+6HCl═2FeCl3+3H2O (4)①NaOH ②NaOH Ca(OH)2
(5)2Al+2NaOH+2H2O═2NaAlO2+3H2↑
点评:要想解答好这类题目,首先,要理解和熟记物质的鉴别、推断及其方法,以及与之相关的知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意等,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目
用化学实验证明了化学反应中质量守恒定律的科学家是( )
| A、波义耳 | B、拉瓦锡 |
| C、门捷列夫 | D、汤姆生 |
只用一种试剂就能区别HCl、BaCl2、KNO3三种溶液,这种试剂是( )
| A、碳酸钾溶液 | B、稀硫酸 |
| C、硝酸银溶液 | D、氯化钠溶液 |
绿色能源不会产生或残留对环境造成污染的物质,下列能源中不能称为绿色能源的( )
| A、煤 | B、氢能 | C、风能 | D、太阳能 |
区别下列各组物质,所选择试剂(括号内)错误的是( )
| A、炭粉与氧化铜(稀盐酸) |
| B、氢氧化钠溶液与澄清石炭水(无色酚酞溶液) |
| C、硬水与软水(肥皂水) |
| D、氯化铵与氯化钾(熟石灰) |
雄伟壮观的国家大剧院主体建筑表面安装了近2万块(Ti)金属板.已知Ti原子核内有22个质子,则下列叙述不正确的是( )
| A、钛原子核外有22个电子 |
| B、Ti4+核外有26个电子 |
| C、TiO2是氧化物 |
| D、钛原子核电荷数是22 |
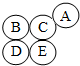 如图所示,五个圆中的A、B、C、D、E分别表示铁、氧化铁、硫酸铜溶液、稀盐酸、氢氧化钠溶液中的五种物质,用两圆相切表示两种物质可以发生反应,没有相切的表示彼此间不会反应,请回答下列问题:
如图所示,五个圆中的A、B、C、D、E分别表示铁、氧化铁、硫酸铜溶液、稀盐酸、氢氧化钠溶液中的五种物质,用两圆相切表示两种物质可以发生反应,没有相切的表示彼此间不会反应,请回答下列问题: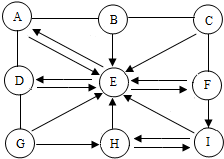 如图中的A-I所表示物质均为初中化学常见的纯净物.其中A、D是非金属单质;B、E、H 是氧化物;B中氧元素质量分数为20%且为黑色粉末;G是天然气的主要成分;C、F、I是三种不同类别的无机化合物;F常用于改良酸性土壤.图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系.(部分反应物或生成物已略去)
如图中的A-I所表示物质均为初中化学常见的纯净物.其中A、D是非金属单质;B、E、H 是氧化物;B中氧元素质量分数为20%且为黑色粉末;G是天然气的主要成分;C、F、I是三种不同类别的无机化合物;F常用于改良酸性土壤.图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系.(部分反应物或生成物已略去)