题目内容
11.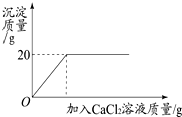 将一定质量的碳酸钠粉末溶于200g水中配制成溶液,向该溶液中加入20%的氯化钙溶液至不再产生白色沉淀,所得产生沉淀的质量与加入氯化钙溶液的质量关系如图所示,试计算:恰好完全反应不再产生白色沉淀时所用氯化钙溶液的质量.
将一定质量的碳酸钠粉末溶于200g水中配制成溶液,向该溶液中加入20%的氯化钙溶液至不再产生白色沉淀,所得产生沉淀的质量与加入氯化钙溶液的质量关系如图所示,试计算:恰好完全反应不再产生白色沉淀时所用氯化钙溶液的质量.
分析 碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,根据沉淀的质量可以计算氯化钙的质量,进一步可以计算恰好完全反应时所需氯化钙溶液的质量.
解答 解:设恰好完全反应时所需氯化钙的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl,
111 100
x 20g
$\frac{111}{x}$=$\frac{100}{20g}$,
x=22.2g,
恰好完全反应时所需氯化钙溶液的质量为:$\frac{22.2g}{20%}$=111g,
答:恰好完全反应时所需氯化钙溶液的质量为111g.
点评 本题属于数形结合型计算,由表示反应过程的曲线获得恰好完全反应即曲线的折点时的相关数据时,体现对问题的分析能力.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
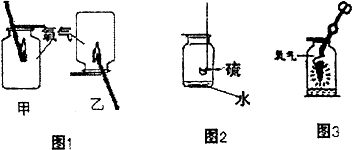
1.某课外活动小组的同学将16克氧化铜和过量的炭粉均匀混合,用如图1所示装置进行实验.图中铁架台等装置已略去.请回答有关问题:
(1)实验中最多能得到铜12.8克.

(2)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前.后测得的数据如下:
分析数据发现,反应中消耗碳和氧元素的质量大于(填“大于”或“小于”或“等于”生成二氧化碳的质量.下列4项中跟这一结果有关的有哪几项?AB.(填编号)
A.装置中还有一部分CO2未被NaOH溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(3)有同学认为用图2所示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2.N2和H2三种气体中,X应选择哪一种气体?N2.
(1)实验中最多能得到铜12.8克.

(2)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前.后测得的数据如下:
| 装置 | 反应前 | 反应后 |
| A | 试管的质量36.2 克 氧化铜和炭粉混合物的质量20.0克 | 试管和固体物质的质量54.8 克 |
| B | 反应后瓶内液体比反应前增重1.1 克 | |
A.装置中还有一部分CO2未被NaOH溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(3)有同学认为用图2所示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2.N2和H2三种气体中,X应选择哪一种气体?N2.
2.下列物质不属于金属材料的是( )
| A. | 青铜 | B. | 生铁 | C. | 赤铁矿 | D. | 钢 |
19.下列各项实验操作正确的是( )
| A. | 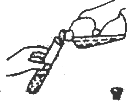 | B. | 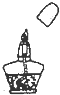 | C. | 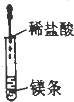 | D. | 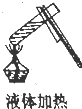 |
6.某固体粉末可能由氢氧化钠、氢氧化钙、碳酸钠和碳酸钙中的一种或几种组成,现进行如下实验:①取少量固体加入足量的水,搅拌,有不溶物;②过滤,向滤液中加入盐酸,有气泡产生.下列对固体粉末成分的判断中,不正确的是( )
| A. | 一定有碳酸钠 | B. | 可能有氢氧化钠 | C. | 一定有碳酸钙 | D. | 可能有氢氧化钙 |
16.在蜡烛燃烧过程中,发生的变化有( )
| A. | 只有物理变化 | B. | 可能有物理变化,一定有化学变化 | ||
| C. | 只有化学变化 | D. | 既有物理变化,又有化学变化 |