题目内容
12.向一定量氢氧化钠和碳酸钠的固体混合物中加入100g质量分数为7.3%的稀盐酸,恰好完全反应,下列有关物质质量计算结果的表述正确的是( )| A. | 反应后生成二氧化碳的质量可能为4.4g | |
| B. | 反应后生成氯化钠的质量一定为11.7g | |
| C. | 反应后生成水的质量可能为3.6g | |
| D. | 固体混合物的质量可能为10g |
分析 氢氧化钠和稀盐酸反应生成氯化钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据稀盐酸质量及其质量分数可以计算反应生成氯化钠的质量.
解答 解:设反应生成氯化钠质量为x,
100g质量分数为7.3%的稀盐酸中氯化氢质量为:100g×7.3%=7.3g,
NaOH+HCl═NaCl+H2O,Na2CO3+2HCl═2NaCl+H2O+CO2↑可知,HCl═NaCl,
HCl═NaCl,
36.5 58.5
7.3g x
$\frac{36.5}{7.3g}$=$\frac{58.5}{x}$,
x=11.7g,
由反应的化学方程式及其生成氯化钠的质量可知,生成二氧化碳的质量小于4.4g,生成水的质量小于3.6g;
生成11.7g氯化钠时,单独消耗氢氧化钠的质量是8g,单独消耗碳酸钠的质量是10.6g,因此固体混合物的质量可能为10g,
由分析可知,BD选项是正确的.
故选:BD.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
3.人体一些液体的正常pH范围如下,其中酸性最强的是( )
| A. | 胆汁7.1-7.3 | B. | 胃液0.9-1.5 | C. | 血浆7.35-7.45 | D. | 尿液4.7-8.4 |
7.下列物质的用途中,利用其化学性质的是( )
| A. | 液氮用作冷冻剂 | B. | 干冰用于人工降雨 | ||
| C. | 氧气用于气焊 | D. | 稀有气体可作电光源 |
7.下列物质中属于碱的是( )
| A. | 纯碱 | B. | 烧碱 | C. | 小苏打 | D. | 生石灰 |

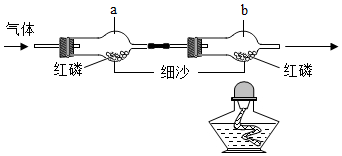 同学们在实验室中按图所示装置探究燃烧的条件.(夹持仪器已略去)
同学们在实验室中按图所示装置探究燃烧的条件.(夹持仪器已略去)