题目内容
9.某课外活动小组为了测定一批石灰石中碳酸钙的质量分数,将石灰石样品研成粉末,然后取一定量的石灰石粉末与过量稀盐酸充分反应(假设石灰石中的杂质既不和酸反应,也不溶于水),过滤、洗涤、干燥后称量滤渣质量的数据如下表:| 实验序号 | 样品的质量/g | 滤渣的质量/g |
| 第一次 | 3.4 | 0.3 |
| 第二次 | 3.6 | 0.4 |
| 第三次 | 5.0 | 0.5 |
(2)若利用题(1)的结果,煅烧100t这种石灰石,理论上最多能得到氧化钙多少吨?(结果精确到0.1t)
分析 (1)求算三次数值的平均即可,杂质是石灰石中碳酸钙之外的全部成分.
(2)根据第一步的计算结果和石灰石100t,结合化学方程式计算.
解答 解:
(1)样品中碳酸钙的质量分数为$\frac{3.4g+3.6g+5.0g-0.3g-0.4g-0.5g}{3.4g+3.6g+5.0g}$×100%=90%
设煅烧100t含碳酸钙90%的石灰石,得到的氧化钙的质量为x(不能理解为含杂质的生石灰)
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
100t×90% x
$\frac{100}{56}$=$\frac{100t×90%}{x}$
x=50.4t
答:(1)该样品中碳酸钙质量分数的平均值为:90%.
(2)若利用题(1)的结果,煅烧100t这种石灰石,理论上最多能得到氧化钙50.4t
点评 根据化学方程式计算时只有纯净物的量才能直接进入计算,其次要注意使用准确的相对分子质量等.过程要完整.

练习册系列答案
相关题目
20.碳酸氢钠用于焙制糕点在270℃时分解2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,现取16.8克NaHCO3,在敞口试管中加热到质量不在减少为止,减少的质量为( )
| A. | 4.4 g | B. | 6.2 g | C. | 8.8 g | D. | 10.6 g |
17.根据如图所示实验现象,关于氧气和二氧化碳的性质说法错误的是( )
| A. | 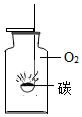 O2具有助燃性 | B. | 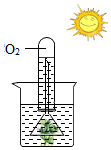 O2不易溶于水 | ||
| C. | 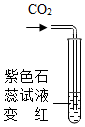 CO2具有酸性使石蕊变色 | D. | 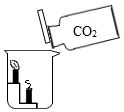 CO2密度比空气大 |
7.下列有关实验操作和现象说法中合理的是( )
| A. | 实验室用肥皂水来区分硬水和蒸馏水 | |
| B. | 用尝味道的方法区分实验室中的食盐和蔗糖 | |
| C. | 磷在氧气中燃烧,产生大量的雾,并有白色固体生成 | |
| D. | 铁丝在空气中燃烧,火星四射,并有黑色固体生成 |
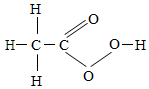 自3月31日中国发生H7N9禽流感病毒疫情,H7N9禽流感疫情发展成为社会关注热点.对环境进行消毒是预防最好的一种方法,其中过氧乙酸溶液是一种很好的消毒液,可以杀灭一切微生物,对病毒、细菌、真菌及芽孢均能迅速杀,过氧乙酸的结构模型如图.
自3月31日中国发生H7N9禽流感病毒疫情,H7N9禽流感疫情发展成为社会关注热点.对环境进行消毒是预防最好的一种方法,其中过氧乙酸溶液是一种很好的消毒液,可以杀灭一切微生物,对病毒、细菌、真菌及芽孢均能迅速杀,过氧乙酸的结构模型如图.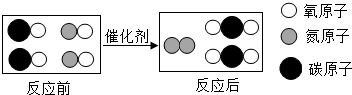
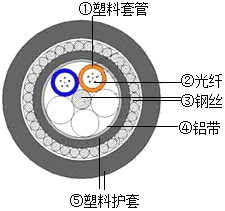 随着网络时代的发展,安徽省大力推广光纤宽带上网.如图是光缆的结构示意图,其中的光纤由高纯度的二氧化硅制成.
随着网络时代的发展,安徽省大力推广光纤宽带上网.如图是光缆的结构示意图,其中的光纤由高纯度的二氧化硅制成.