题目内容
把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如下表所示,下列说法正确的是( )
| 物质 | A | B | C | D |
| 反应前的质量/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后的质量/g | 待测 | 19.4 | 0 | 3.6 |
|
| A. | 物质C一定是化合物,物质D可能是单质 |
|
| B. | 反应后密闭容器中A的质量为19.7 g |
|
| C. | 反应中,物质B和物质D质量比为87:36 |
|
| D. | 该反应为化合反应 |
| 质量守恒定律及其应用.. | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | 根据质量守恒定律,可分析先B、C、D三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定A是反应物还是生成物,进而可以确定反应类型. |
| 解答: | 解:由表中数据分析可知,反应前后,B的质量增加了10.7g,故B是生成物,参加反应的B的质量为10.7g;同理可以确定C是反应物,参加反应的C的质量为21.6g;D的质量增加了3.2g,故D是生成物,生成D的质量为3.2g;由质量守恒定律,A应是生成物,且生成的A的质量为21.6g﹣10.7g﹣3.2g=7.7g. A、该反应的反应物为C,生成物是A、B、D,因此物质C一定是化合物,物质D可能是单质,故选项说法正确; B、生成的A的质量为7.7g,则待测的值为7.7g+19.7g=27.4g,故选项说法错误; C、由质量守恒定律,物质B和物质D质量增加的比为(19.4g﹣8.7g):(3.6g﹣0.4g)=107:32,故选项说法错误; D、该反应的反应物为C,生成物是A、B、D,符合“一变多”的特征,属于分解反应,故选项说法错误; 故选:A. |
| 点评: | 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据、灵活运用质量守恒定律. |

胆矾是一种蓝色晶体,化学式是CuSO4•5H2O,胆矾受热时容易失去结晶水,成为白色的无水硫酸铜,在工业上精炼铜、镀铜等都要应用胆矾.上述对胆矾的描述没有涉及到的是( )
|
| A. | 制法 | B. | 物理性质 | C. | 化学性质 | D. | 用途 |
下列各组物质中,前者属于纯净物,后者属于混合物的是( )
|
| A. | 冰水混合物,五氧化二磷 | B. | 矿泉水,河水 |
|
| C. | 二氧化碳,澄清石灰水 | D. | 净化后的空气,受污染的空气 |
过氧化钠(化学式为Na2O2,其中Na元素显+1价)是潜水艇中的制氧剂,它是一种淡黄色粉末,能与物质R反应生成氧气,反应的化学方程式为:2Na2O2+2R═2Na2CO3+O2,则下列有关判断中,错误的是( )
|
| A. | Na2O2中氧元素化合价为﹣1价 | B. | R的化学式为CO2 |
|
| C. | Na2CO3的相对分子质量为106 | D. | Na2O2中含有氧分子 |
已知2A+3B=C+3D,用足量的A和49g B恰好完全反应,其生成57g C和1g D,,若B的相对分子质量为98,则A的相对分子质量为( )
|
| A. | 16 | B. | 27 | C. | 44 | D. | 56 |
下列粒子不显电性的是( )
|
| A. | 质子 | B. | 电子 | C. | 原子核 | D. | 分子 |
 .吸附 B.沉降 C.过滤 D.蒸馏
.吸附 B.沉降 C.过滤 D.蒸馏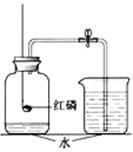 橡皮管。点燃红磷伸入瓶中并塞上瓶塞。待红磷熄灭后,
橡皮管。点燃红磷伸入瓶中并塞上瓶塞。待红磷熄灭后, 打开弹
打开弹