题目内容
500吨的大理石高温煅烧,至质量不再减少为止,得剩余固体302吨,则:
(1)根据质量守恒定律可知,该过程中产生二氧化碳 吨.
(2)所得的剩余固体中,杂质的质量分数为?(CaCO3=100 CO2=44 CaO=56 )
(1)根据质量守恒定律可知,该过程中产生二氧化碳
(2)所得的剩余固体中,杂质的质量分数为?(CaCO3=100 CO2=44 CaO=56 )
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:反应前后固体物质的质量差即为生成二氧化碳的质量;
大理石在高温条件下分解生成氧化钙和二氧化碳,根据二氧化碳的质量可以计算氧化钙的质量,进一步可以计算杂质的质量分数.
大理石在高温条件下分解生成氧化钙和二氧化碳,根据二氧化碳的质量可以计算氧化钙的质量,进一步可以计算杂质的质量分数.
解答:解:(1)根据质量守恒定律可知,该过程中产生二氧化碳为:500t-302t=198t.
故填:198.
(2)解:设生成氧化钙的质量为x,
CaCO3
CaO+CO2↑,
56 44
x 198t
=
,
x=252t,
则所得的剩余固体中,杂质的质量分数为:
×100%≈16.6%,
答:所得的剩余固体中,杂质的质量分数为16.6%.
故填:198.
(2)解:设生成氧化钙的质量为x,
CaCO3
| ||
56 44
x 198t
| 56 |
| 44 |
| x |
| 198t |
x=252t,
则所得的剩余固体中,杂质的质量分数为:
| 302t-252t |
| 302t |
答:所得的剩余固体中,杂质的质量分数为16.6%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
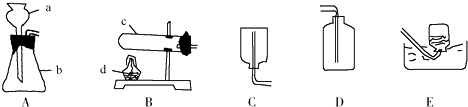
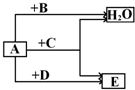 现有A、B、C、D、E五种常见的气体,它们之间存在如图所示转化关系,其中A、B是单质,C是最简单的有机物,E能使澄清石灰水变浑浊.
现有A、B、C、D、E五种常见的气体,它们之间存在如图所示转化关系,其中A、B是单质,C是最简单的有机物,E能使澄清石灰水变浑浊.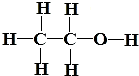 .乙醇是无色、透明、有香味、易挥发的液体,密度比水小,熔点-117.3℃,沸点78.5℃,极易溶于水.具有可燃性,能与金属钠发生反应生成氢气.依据上述信息回答下列问题:
.乙醇是无色、透明、有香味、易挥发的液体,密度比水小,熔点-117.3℃,沸点78.5℃,极易溶于水.具有可燃性,能与金属钠发生反应生成氢气.依据上述信息回答下列问题: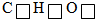 (右下角方框内填上原子个数);
(右下角方框内填上原子个数); 在如图所示电解水的实验中:
在如图所示电解水的实验中: