题目内容
13.阅读下面的科普短文.冬季在户外活动时,可以使用取暖贴保暖,它可以防止肌肉因过冷而引起的紧张,防止手部冻伤,缓解腰痛、腿痛、肩痛和其他生理病痛.
在70年代,人们基于化 学知识发明了取暖贴.不用火、电、水或其他能源,撕开外袋即可发热,可保持8-18小时左右(平均温度52℃).因为不使用火,小孩和老人都可安全使用.
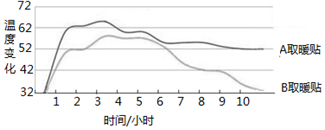
取暖贴的反应原理为利用 原电池加快氧化反应速度,将化学能转变为热能.因为产品中的物质在使用前不能接触空气,所以袋子材质要很特别,由原料层,明胶层和无纺布袋组成.原料层包含铁粉、蛭石、活性炭、氯化钠、水等,无毒、无副作用;无纺布袋是采用微孔透气膜制作的;它还得有一个常规不透气的外袋--明胶层.在使用时,去掉外袋,让内袋(无纺布袋)暴露在空气里,空气中的氧气通过透气膜进入里面,铁粉在空气中与氧气、水发生反应生成氢氧化亚铁,氢氧化亚铁再被氧化成氢氧化铁,氢氧化铁分解为氧化铁,该过程放出热量.放热的时间和温度就是通过透气膜的透氧速率进行控制的.如果透氧太快,热量一下子就放掉了,而且还有可能烫伤皮肤.如果透氧太慢,就没有什么温度了.为了使温度能够持续更长,产品使用了矿物材料蛭石来保温.下图是两种取暖贴的发热时间和温度的变化情况.
 使用取暖贴还需要注意不能直接接触 皮肤,以免温度过高烫伤皮肤.同时在晚上睡觉的时候也不能使用,避免在同一位置长时间使用,并注意皮肤状况,如有异常立即取下.
使用取暖贴还需要注意不能直接接触 皮肤,以免温度过高烫伤皮肤.同时在晚上睡觉的时候也不能使用,避免在同一位置长时间使用,并注意皮肤状况,如有异常立即取下.依据文章内容回答下列问题.
(1)任意写出取暖贴原料层中两种成分的化学式NaCl、Fe、C等.
(2)原料层中蛭石的作用是保温.
(3)“取暖贴”放出的热量是化学变化产生的(填“物理”或“化学”).
(4)下列关于取暖贴的说法正确的是BCD.
A.总反应为:2Fe+3H2O═2Fe(OH)3
B.使用取暖贴不能直接接触皮肤
C.根据图象判断可知,A取暖贴的保温效果好于B
D.取暖贴在使用前必须密封保存
(5)请对取暖贴剩余物的处理提出一条合理化建议回收利用.
分析 (1)取暖贴原料层中的物质及其化学式的写法来分析;
(2)根据题干信息:用蛭石来保温来分析;
(3)根据是否生成新物质来分析;
(4)根据题干信息来分析;
(5)根据取暖贴剩余物来分析.
解答 解:(1)原料层包含铁粉、蛭石、活性炭、氯化钠、水等,铁的化学式为Fe;氯化钠的化学式为NaCl;活性炭的化学式C;故填:NaCl、Fe、C等;
(2)为了使温度能够持续更长,产品使用了矿物材料蛭石来保温.故填:保温;
(3)“取暖贴”中的铁粉生锈放出热量,有新物质生成,发生的属于化学变化;故填:化学;
(4)A.铁粉在空气中与氧气、水发生反应生成氢氧化亚铁,氢氧化亚铁再被氧化成氢氧化铁,氢氧化铁分解为氧化铁,故错误;
B.使用取暖贴不能直接接触皮肤,以免温度过高烫伤皮肤,故正确;
C.根据图象判断可知,A放热多,温度持续时间长,所以A取暖贴的保温效果好于B,故正确;
D.因为产品中的物质在使用前不能接触空气,所以取暖贴在使用前必须密封保存,故正确;
故填:BCD;
(5)取暖贴剩余物碳、蛭石等物质可以回收利用;故填:回收利用(合理即可).
点评 本题考查了暖贴的使用原理,解答时根据铁锈蚀的条件来分析解答.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
3.有一白色固体,只知它是CaCO3、无水CuSO4、Ca(OH)2、Na2CO3、NaOH中的一种或几种.某兴趣小组同学为探究白色固体的成份,实验如下:取样,加适量水充分搅拌,过滤,得白色沉淀和无色溶液.据此判断,该白色固体中一定没有无水CuSO4.
该小组同学对所得白色沉淀继续进行实验探究:
【提出问题】所得白色沉淀的成份是什么?
【猜想与假设】请你帮助完成猜想三.
猜想一:Ca(OH)2猜想二:CaCO3猜想三:Ca(OH)2和CaCO3
【实验验证】请你完成填空.
【反思与拓展】
(1)所得白色沉淀是Ca(OH)2的原因可能是氢氧化钙是微溶物质.
(2)分析得出该白色固体中没有Na2CO3,理由是实验已证明白色固体中有Ca(OH)2,若有Na2CO3,向所得白色沉淀中加入稀盐酸会有气体产生,这与实验现象不符.
(3)分析得出该白色固体中可能有NaOH,请你设计一个实验方案,证明它是否存在?方案1:取样,加入适量水溶解,用温度计测量溶液温度是否升高.
或方案2:取样,放置在烧杯中,观察是否发生潮解..
该小组同学对所得白色沉淀继续进行实验探究:
【提出问题】所得白色沉淀的成份是什么?
【猜想与假设】请你帮助完成猜想三.
猜想一:Ca(OH)2猜想二:CaCO3猜想三:Ca(OH)2和CaCO3
【实验验证】请你完成填空.
| 实验操作 | 实验现象 | 实验结论 |
| 取白色沉淀少量,加入足量 稀盐酸 | 白色沉淀消失,无气泡产生 | 猜想一成立. 从而确定了该白色固体中一定有Ca(OH)2 |
(1)所得白色沉淀是Ca(OH)2的原因可能是氢氧化钙是微溶物质.
(2)分析得出该白色固体中没有Na2CO3,理由是实验已证明白色固体中有Ca(OH)2,若有Na2CO3,向所得白色沉淀中加入稀盐酸会有气体产生,这与实验现象不符.
(3)分析得出该白色固体中可能有NaOH,请你设计一个实验方案,证明它是否存在?方案1:取样,加入适量水溶解,用温度计测量溶液温度是否升高.
或方案2:取样,放置在烧杯中,观察是否发生潮解..
4.采取正确的措施,能够避免火灾发生或减少灾害损失.下列灭火方法不恰当的是( )
| A. | 油锅起火--用锅盖盖灭 | B. | 酒精灯着火--用湿抹布盖灭 | ||
| C. | 汽车油箱着火--用水浇灭 | D. | 森林起火--砍伐树木形成隔离带 |
1.下列实验方案,不能达到实验目的是( )
| 选项 | 实验方案 | 实验目的 |
| A | 将粗盐研碎,溶解、过滤、蒸发 | 除去粗盐中难溶性杂质 |
| B | 将气体点燃 | 除去CO2中的少量CO |
| C | 分别取少量溶液,滴加碳酸钠溶液 | 鉴别石灰水和NaOH溶液 |
| D | 将气体通入浓硫酸 | 除去O2中少量的水蒸气 |
| A. | A | B. | B | C. | C | D. | D |
8.同学们来到了“自制酸碱指示剂”展台.
(1)上述两种植物的汁液不适合做酸碱指示剂的是胡萝卜.
(2)将紫甘蓝汁液滴入稀硫酸中,溶液呈红 色.
| 植物的汁液 | 白醋 | 蒸馏水 | 氢氧化钠溶液 |
| 紫甘蓝 | 红色 | 蓝紫色 | 绿色 |
| 胡萝卜 | 橙色 | 橙色 | 橙色 |
(2)将紫甘蓝汁液滴入稀硫酸中,溶液呈红 色.
18.下列化学方程式书写正确的是( )
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | Fe2O3+3CO═2Fe+3CO2 | D. | KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2 |
5.科学家最新发现,通过简单的化学反应,可以将树木纤维素转变为超级储能装置,该反应的微观示意图如图,下列说法正确的是( )
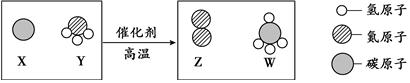

| A. | Y是由四种元素组成的化合物 | |
| B. | 该反应中X、Z两种物质的质量比为3:14 | |
| C. | 该反应中生成的Z和W两物质的分子个数比为1:1 | |
| D. | 参加反应的Y中氮元素的质量一定等于生成Z的质量 |
2.在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如表所示.下列有关说法不正确的是( )
| 物 质 | a | b | c | d |
| 反应前的质量/g | 30 | 20 | 8 | 14 |
| 反应后的质量/g | x | y | 0 | 10 |
| A. | 参加反应的c与d的质量比为2:1 | B. | x+y=62 | ||
| C. | x的取值范围必须是0≤x≤30 | D. | 当y≤20时,该反应一定是化合反应 |