题目内容
18.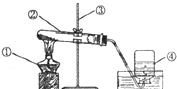 如图所示是实验室用高锰酸钾制取氧气的装置图.请根据图示及所学知识回答下列问题.
如图所示是实验室用高锰酸钾制取氧气的装置图.请根据图示及所学知识回答下列问题.(1)写出有标号的仪器名称:①酒精灯;②试管
(2)写出加热高锰酸钾制氧气的文字表达式高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)实验室制氧气有以下步骤;
①撤去酒精灯;②检查装置气密性;
③点燃酒精灯加热;④收集气体;⑤撤出水槽中的导管;
⑥往试管中装入高锰酸钾,并将一小团棉花放在试管口;
⑦将装置固定在铁架台上.操作的正确顺序应该是②⑥⑦③④⑤①
(4)可用装置图中所示方法收集氧气的原因是氧气不易溶于水,还可以用向上排空气法收集氧气,因为氧气的密度比空气的密度大,若用此方法收集,检验氧气收集满的方法是将带火星的木条放在集气瓶口,木条熄灭,则证明已满;
(5)高锰酸钾制氧气,需要在试管口放一团棉花,目的是:防止高锰酸钾颗粒进入导气管
(6)加热时要先预热,目的是:防止试管受热不均匀而炸裂
(7)加热时试管口略向下倾斜的原因是:防止冷凝水倒流引起试管的炸裂
(8)用排水法收集氧气,开始收集气体的适宜时刻是:气泡连续、均匀冒出时开始收集
(9)实验结束时,要先把导管从水槽中取出,再移开酒精灯,这样做的目的是:防止水倒吸入热的试管引起试管炸裂
(10)收集满氧气的集气瓶应正(填“正”或“倒”)放在桌面上,是因为氧气的密度比空气的密度大.
分析 (1)根据实验室常用仪器解答;
(2)根据加热高锰酸钾制氧气的原理解答;
(3)根据实验室制氧气的步骤解答;
(4)根据氧气不易溶于水,密度比空气的密度大,因此可以用排水法和向上排空气法收集解答;
(5)根据高锰酸钾制氧气的注意事项解答;
(6)根据给试管加热时的注意事项解答;
(7)根据给试管加热时的注意事项解答;
(8)运用高锰酸钾制取氧气的基本步骤和操作时注意事项解答.
(9)运用高锰酸钾制取氧气的基本步骤和操作时注意事项解答.
(10)根据氧气的性质解答.
解答 解:
(1)根据实验室常用仪器可知:①酒精灯;②试管;
(2)加热高锰酸钾制氧气生成锰酸钾、二氧化锰、氧气,反应的文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(3)实验操作步骤是:检查装置的气密性、装药品、固定、给试管加热、收集气体、从水槽中移出导管、熄灭酒精灯.故答案为:②⑥⑦③④⑤①;
(4)可用装置图中所示方法收集氧气的原因是氧气不易溶于水,氧气的密度比空气的密度大,因此还可以用向上排空气法收集;若用此方法收集,检验氧气收集满的方法是将带火星的木条放在集气瓶口,木条熄灭,则证明已满;
(5)高锰酸钾制氧气,需要在试管口放一团棉花,目的是:防止高锰酸钾颗粒进入导气管;
(6)加热时要先预热,目的是:防止试管受热不均匀而炸裂;
(7)加热时试管口略向下倾斜的原因是:防止冷凝水倒流引起试管的炸裂;
(8)用排水法开始收集氧气的适宜时刻是:气泡连续、均匀冒出时开始收集,防止收集的气体不纯;
(9)用排水法收集氧气完毕后,应先移导管后熄灯,防止水倒吸入热的试管引起试管炸裂;
(10)收集满氧气的集气瓶应正放在桌面上,是因为氧气的密度比空气的密度大.
答案:
(1)①酒精灯;②试管;
(2)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(3)②⑥⑦③④⑤①;
(4)氧气不易溶于水;向上排空气法;氧气的密度比空气的密度大;将带火星的木条放在集气瓶口,木条熄灭,则证明已满;
(5)防止高锰酸钾颗粒进入导气管;
(6)防止试管受热不均匀而炸裂;
(7)防止冷凝水倒流引起试管的炸裂;
(8)气泡连续、均匀冒出时开始收集;
(9)防止水倒吸入热的试管引起试管炸裂;
(10)正;的密度比空气的密度大.
点评 本考点主要考查仪器的名称、氧气的制取装置的错误之处,同时也考查了操作步骤和化学方程式的书写,综合性比较强.要加强记忆有关的知识点,并能综合应用.本考点是中考的重要考点之一,主要出现在实验题中.

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【提出问题】(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】(1)假黄金通常是黄铜(Cu-Zu合金) (2)钯(Pd)呈银白色,有金属光泽,可用作饰品
【实验药品 钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】(1)鉴别黄金样品的真假:取黄金样品于试管中,滴加稀盐酸后,观察黄金样品表面有气泡产生,该气体是氢气(填名称),说明此样品为假(填“真”或“假”)黄金.
(2)探究钯的金属活动性:依据生活经验,同学们猜测钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 把钯浸入硝酸银溶液中 | 无明显现象 | 钯的活动性比银弱 |
| 把铂浸入氯化钯溶液中 | 无明显现象 | 钯的活动性比铂强 |
【废液处理】(1)转化成沉淀.小组同学所有液体倒入废液缺缸中,出现白色沉淀.写出产生该现象的化学方程式:ZnCl2+2AgNO3=2AgCl↓+Zn(NO3)2(写出一个即可).
(2)通过科学合理的方法进一步回收金属钯.
| A. | N2中混有O2(通过灼热的木炭) | B. | KOH中混有KCl(加适量稀盐酸) | ||
| C. | 稀盐酸中混有硫酸(加硝酸钡溶液) | D. | CaO中混有CaCO3(高温煅烧) |
| 20摄氏度一些物质的溶解度(g) | |||
| 氯化钠 | 氯化铵 | 碳酸氢钠 | 碳酸氢铵 |
| 35.9 | 37.2 | 9.6 | 21.7 |
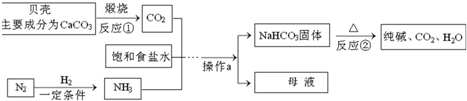
①NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓ ②2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O 请回答:
(1)反应①的化学方程式CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
(2)经过操作a析出晶体后的母液是的HCO3的饱和(填“饱和”或“不饱和”)溶液.写出母液中所有溶质的化学式:NaHCO3、NH4Cl、NaCl
(3)该厂母液中氯化铵(写名称)可作化肥中的氮肥,它也可与Ca(OH)2在加热时发生反应,写出该反应的化学方程式:Ca(OH)2+2NH4Cl=CaCl2+H2O+CO2↑.
(4)此流程中可以循环利用的物质是CO2(写化学式)

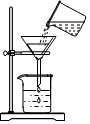 将含有少量泥沙的食盐提纯并配制食盐水溶液,某同学进行以下实验操作,回答下列问题.
将含有少量泥沙的食盐提纯并配制食盐水溶液,某同学进行以下实验操作,回答下列问题.