题目内容
10.每四年一次的奥运会都要传递火炬,火炬外壳主要采用轻薄高品质的铝合金材料,下半部喷涂高触感红色塑胶漆,手感舒适不易滑落,火炬所用燃料为丙烷.某中学的阳阳和几个同学在看完传递仪式后,就想丙烷(C3H8)作为奥运火炬使用的燃料,其燃烧后的产物是什么?阳阳和她的同学选择了如下装置(铁架台等装已置已略去),对丙烷在氧气中燃烧后的气体进行了检测.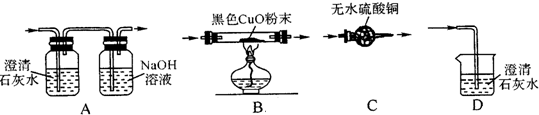
①经分析,丙烷燃烧后的气体可能含有CO、CO2和H2O;
②将上述装置按一定顺序连接完整,使之尽可能检测出丙烷燃烧后的产物.你设计的连接顺序为:燃烧后的气体→C→A→B→D.
③该小组的同学按合理的连接顺序进行检测,实验过程中观察到的部分现象如下:A装置中的澄清石灰水变浑浊,C装置中的无水硫酸铜变蓝,D装置中的澄清石水无明显现象.分析可知,丙烷在氧气中燃烧后的产物为CO2、H2O.
④A装置中的NaOH溶液的作用是完全吸收二氧化碳.
分析 (2)根据丙烷含有的元素,结合质量守恒定律来解答;
(3)根据实验现象来判断甲醇燃烧的产物,由于氢元素的存在,肯定生成水;
(4)氢氧化钠溶液是用来除去酸性气体.
解答 解:(2)丙烷中含有碳元素、氢元素和氧元素,在燃烧时可能产生一氧化碳、二氧化碳和水等物质,检验一氧化碳可以用氧化铜,检验二氧化碳可以用澄清石灰水,检验水常用无水硫酸铜,考虑到一氧化碳能够反应生成二氧化碳,所以应该先检验二氧化碳,然后鉴别一氧化碳,而气体通过澄清石灰水时会带出水蒸气,故应该最先检验水,然后是二氧化碳,最后检验一氧化碳;因此顺序为:燃烧后的气体→C→A→B→D;
(2)根据A中左边石灰水变浑浊可知生成了二氧化碳,C装置中的无水硫酸铜变蓝,可知生成了水,根据D中石灰水无明显现象可知没有生成一氧化碳,故可以知道甲醇燃烧后的产物为二氧化碳和水;
(3)实验要验证一氧化碳还原氧化铜的产物,所以要除去前面生成的二氧化碳气体对结果的干扰,故装置A中氢氧化钠溶液的作用就完全吸收二氧化碳.
答案:
(1)C→A;
(2)CO2、H2O;
(3)完全吸收二氧化碳.
点评 本题考查了常见气体的检验,不要被复杂的装置图吓倒,在明确实验目的基础上,逐个分析就能得出答案,要求熟练掌握质量守恒定律的实质,能够根据质量守恒定律来判断反应后生成的物质.

练习册系列答案
相关题目
18.下列有关碳酸钠性质的描述错误的是( )
| A. | 将其滴入到CaCl2溶液中,会产生白色的沉淀 | |
| B. | 我们不能用紫色石蕊来区别碳酸钠溶液和硝酸钠溶液 | |
| C. | 碳酸钠晶体(Na2CO3•10H2O)属于纯净物 | |
| D. | 当氯化钠溶液中含有少量的碳酸钠时,我们可以通过滴加适量盐酸溶液来除去 |
15.下列是实验室常见的物质,其溶液两两混合,能产生蓝色沉淀的是( )
| A. | BaCl2、Na2SO4 | B. | NaOH、CuSO4 | C. | HCl、Ca(OH)2 | D. | H2SO4、K2CO3 |
2.下列化学实验操作或实验思路正确的是( )
| A. | 在淀粉溶液中加入适量“加碘食盐”发现不变蓝,说明“加碘食盐”中不含单质碘 | |
| B. | 用稀盐酸洗涤试管内壁的油污 | |
| C. | 往某溶液中滴加BaCl2溶液和稀硝酸,产生白色沉淀,则该溶液中一定含有SO42- | |
| D. | 稀释浓硫酸时,把水沿烧杯壁慢慢注入盛浓硫酸的烧杯中并不断搅拌 |
19. 世界上最轻固态材料,在浙大诞生,如图所示,实验室昵称它为“碳海绵”.检测结果显示“碳海绵”还有超强的储电能力;对有机溶剂具有超快、超高的吸附力,是已报道的吸油力最高的材料;放在温度-196℃的液氮中,弹性活力依然;“碳海绵”有很多空隙,可以填充保温材料等物质;它能达到的最小密度为0.16毫克/立方厘米(不包括该物质空隙间的气体);下列关于“碳海绵”的说法不正确的是( )
世界上最轻固态材料,在浙大诞生,如图所示,实验室昵称它为“碳海绵”.检测结果显示“碳海绵”还有超强的储电能力;对有机溶剂具有超快、超高的吸附力,是已报道的吸油力最高的材料;放在温度-196℃的液氮中,弹性活力依然;“碳海绵”有很多空隙,可以填充保温材料等物质;它能达到的最小密度为0.16毫克/立方厘米(不包括该物质空隙间的气体);下列关于“碳海绵”的说法不正确的是( )
 世界上最轻固态材料,在浙大诞生,如图所示,实验室昵称它为“碳海绵”.检测结果显示“碳海绵”还有超强的储电能力;对有机溶剂具有超快、超高的吸附力,是已报道的吸油力最高的材料;放在温度-196℃的液氮中,弹性活力依然;“碳海绵”有很多空隙,可以填充保温材料等物质;它能达到的最小密度为0.16毫克/立方厘米(不包括该物质空隙间的气体);下列关于“碳海绵”的说法不正确的是( )
世界上最轻固态材料,在浙大诞生,如图所示,实验室昵称它为“碳海绵”.检测结果显示“碳海绵”还有超强的储电能力;对有机溶剂具有超快、超高的吸附力,是已报道的吸油力最高的材料;放在温度-196℃的液氮中,弹性活力依然;“碳海绵”有很多空隙,可以填充保温材料等物质;它能达到的最小密度为0.16毫克/立方厘米(不包括该物质空隙间的气体);下列关于“碳海绵”的说法不正确的是( )| A. | 在将来的某一天,手机电池带电时间能充分满足人们的需求 | |
| B. | 若海上发生漏油事件,则可以把“碳海绵”撒在海面上迅速吸油 | |
| C. | 若用此材料做成宇航服能抵抗月球晚上零下一百多度的低温 | |
| D. | 相同体积“碳海绵”的质量远小于密度为0.09千克/米3的氢气的质量 |
2.“民以食为天”.下列过程中,发生了化学变化的是( )
| A. | 淘米 | B. | 洗菜 | C. | 糯米酿酒 | D. | 苹果榨汁 |
 如图所示装置,O点是一固定点,活塞连接金属滑片(只滑动不旋转),活塞运动滑动变阻器阻值随之改变.试管内是空气和足量的白磷,烧杯中盛放足量生石灰.闭合电键小灯泡发光后再向烧杯中加入数滴含有酚酞试液的水,试推测:
如图所示装置,O点是一固定点,活塞连接金属滑片(只滑动不旋转),活塞运动滑动变阻器阻值随之改变.试管内是空气和足量的白磷,烧杯中盛放足量生石灰.闭合电键小灯泡发光后再向烧杯中加入数滴含有酚酞试液的水,试推测: