题目内容
8.下列说法不能用质量守恒定律解释的是( )| A. | 镁带在空气中燃烧后,生成物的质量比镁带质量增加了 | |
| B. | 蜡烛完全燃烧后,生成水和二氧化碳的质量之和大于蜡烛质量 | |
| C. | 水的质量和受热变成水蒸汽的质量相等 | |
| D. | 高锰酸钾受热分解后,剩余固体的质量比反应物质量轻 |
分析 质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用于化学变化;物质发生物理变化,则不适用于质量守恒定律来解释;据此进行分析判断.
解答 解:A、镁带燃烧,有新物质氧化镁生成,属于化学变化,能用质量守恒定律解释,故选项错误.
B、蜡烛燃烧,有新物质二氧化碳和水生成,属于化学变化,能用质量守恒定律解释,故选项错误.
C、水受热变成水蒸汽,没有新物质生成,属于物理变化,不能用质量守恒定律解释,故选项正确.
D、高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,有新物质生成,属于化学变化,能用质量守恒定律解释,故选项错误.
故选:C.
点评 质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用于化学变化,掌握化学变化和物理变化的判别是解题的关键.

练习册系列答案
相关题目
19.安徽是农业大省,水稻是安徽省的主要粮食作物之一,如图有关水稻种植过程及其相关应用的叙述中涉及到化学变化的是( )
| A. |  栽种秧苗 | B. |  收割水稻 | C. |  稻谷晾晒 | D. |  稻草发电 |
16.下列物质中,属于纯净物的是( )
| A. | 食用醋 | B. | 干冰 | C. | 含碘盐 | D. | 可乐饮料 |
3.我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法不正确的是( )


| A. | 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 | |
| B. | “侯氏制碱法”制得的碳酸钠俗称为纯碱,它属于盐类物质 | |
| C. | 过滤得到的“母液”为NaHCO3的不饱和溶液 | |
| D. | 沉淀池中的反应物共有6种元素 |
20.九年级化学课,老师拿着一根试管给同学们看,老师说:“试管有什么用途?”张宾说:“生产试管婴儿.”老师继续问:“怎么生产出婴儿?”张宾异想天开地说:“把爸爸和妈妈放在试管里加热.”生产试管婴儿是生物学研究的范畴,但聪明的宝宝们:取一块食盐可以从不同的角度进行研究,你认为以下不是化学研究领域的是( )
| A. | 食盐由什么成分组成 | B. | 食盐的产地在哪里 | ||
| C. | 食盐有什么性质和用途 | D. | 食盐的微观结构如何 |
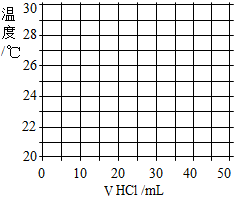
17.
(1)据表可知V盐酸:VNaOH溶液=3:2时,两溶液恰好完全反应.由此可知NaOH溶液的浓度是0.6g/ml.
(2)当V盐酸:VNaOH溶液=1:4时溶液中含有的微粒有H2O、Na+、Cl-,、OH-(填符号).
(3)用铅笔在给定的坐标图上绘出溶液温度与盐酸体积的曲线图.并分析曲线变化的原因:开始时氢氧化钠和盐酸反应放热,溶液温度升高;当盐酸过量后,加入的过量的温度较低的盐酸使溶液温度降低.

| 盐酸的体积V(mL) | 5.0 | 10.0 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 | 40.0 | 45.0 |
| NaOH的体积(mL) | 45.0 | 40.0 | 35.0 | 30.0 | 25.0 | 20.0 | 15.0 | 10.0 | 5.0 |
| 溶液温度t(℃) | 22.2 | 23.3 | 24.6 | 25.8 | 27.0 | 27.8 | 26.1 | 24.4 | 22.8 |
(2)当V盐酸:VNaOH溶液=1:4时溶液中含有的微粒有H2O、Na+、Cl-,、OH-(填符号).
(3)用铅笔在给定的坐标图上绘出溶液温度与盐酸体积的曲线图.并分析曲线变化的原因:开始时氢氧化钠和盐酸反应放热,溶液温度升高;当盐酸过量后,加入的过量的温度较低的盐酸使溶液温度降低.
