题目内容
 某中学综合实践活动小组在进行“诚信商品”研究时,检验商品标签所列成分及含量与实际是否相符.随机取出市售某种“纯碱”样品(成分说明见图),经检验杂质仅是氯化钠,准确称取5.5g该样品,加入足量的氯化钙溶液使其完全反应,其式为:Na2CO3+CaCl2═CaCO3↓+2NaCl2,将反应生成的沉淀物经过滤,洗涤,烘干,干燥后得到白色固体5g.
某中学综合实践活动小组在进行“诚信商品”研究时,检验商品标签所列成分及含量与实际是否相符.随机取出市售某种“纯碱”样品(成分说明见图),经检验杂质仅是氯化钠,准确称取5.5g该样品,加入足量的氯化钙溶液使其完全反应,其式为:Na2CO3+CaCl2═CaCO3↓+2NaCl2,将反应生成的沉淀物经过滤,洗涤,烘干,干燥后得到白色固体5g.(1)计算5.5g样品纯碱(化学式为Na2CO3)的质量;
(2)通过计算判断此纯碱是否可以列入“诚信商品”.
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据反应的化学方程式,生成的沉淀是碳酸钙,根据碳酸钙的质量可以计算出碳酸钠的质量.
(2)根据样品质量求出碳酸钠的质量纯度.
(2)根据样品质量求出碳酸钠的质量纯度.
解答:解:(1)设5.5g样品中纯碱的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 5g
=
x=5.3g
5.5g样品中纯碱(化学式为Na2CO3 )的质量5.3g.
(2)样品中纯碱(化学式为Na2CO3 )的质量分数为:
×100%≈96.4%>95%
所以此纯碱可以列入“诚信商品”.
答:
(1)5.5g样品中纯碱(化学式为Na2CO3 )的质量为5.3g
(2)此纯碱可以列入“诚信商品”.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 5g
| 106 |
| x |
| 100 |
| 5g |
x=5.3g
5.5g样品中纯碱(化学式为Na2CO3 )的质量5.3g.
(2)样品中纯碱(化学式为Na2CO3 )的质量分数为:
| 5.3g |
| 5.5g |
所以此纯碱可以列入“诚信商品”.
答:
(1)5.5g样品中纯碱(化学式为Na2CO3 )的质量为5.3g
(2)此纯碱可以列入“诚信商品”.
点评:本题主要考查学生对物质质量分数的计算能力.学生需正确书写出化学方程式,然后根据化学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题.

练习册系列答案
 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
物质的用途主要利用其化学性质的是( )
| A、干冰用于人工降雨 |
| B、天然气用作燃料 |
| C、氦气用于充霓虹灯 |
| D、活性炭吸附毒气 |
下列实验操作正确的是( )
A、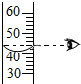 读取液体体积 |
B、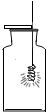 铁丝燃烧 |
C、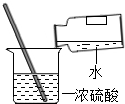 稀释浓硫酸 |
D、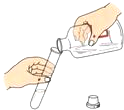 倾倒液体 |
下列生活中的物质属于纯净物的是( )
| A、泪水 | B、天然气 |
| C、大理石 | D、蒸馏水 |
当氧化铜中混有少量木炭粉时,除去木炭粉的方法是( )
| A、隔绝空气加热混合物 |
| B、在氢气流中加热混合物 |
| C、在氧气流中加热混合物 |
| D、加水溶解、过滤 |
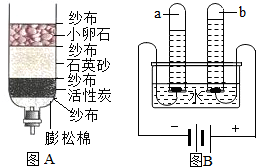 (1)向盛有水的烧杯中加入少量品红,静置一段时间后,溶液逐渐变成红色,此实验主要说明分子的性质是
(1)向盛有水的烧杯中加入少量品红,静置一段时间后,溶液逐渐变成红色,此实验主要说明分子的性质是