题目内容
 如图是一装有氯化镁的试剂瓶,请用化学用语填写下列空格
如图是一装有氯化镁的试剂瓶,请用化学用语填写下列空格(1)细心的小明同学发现标签上的化学式有误,正确的化学式是
(2)标出该物质中氯元素的化合价
(3)已知该物质是由离子构成的,其中的阳离子符号为
(4)该物质可以用金属镁和稀盐酸反应制取同时还生成了氢气,反应的方程式为
分析:(1)在化合物中,元素的化合价代数和为零;
(2)氯化镁中,氯元素的化合价是-1价;
(3)氯化镁是由金属离子和非金属离子构成,金属离子为阳离子;
(4)镁与稀盐酸发生置换反应,生成氯化镁和氢气.
(2)氯化镁中,氯元素的化合价是-1价;
(3)氯化镁是由金属离子和非金属离子构成,金属离子为阳离子;
(4)镁与稀盐酸发生置换反应,生成氯化镁和氢气.
解答:解:(1)氯化镁中,镁元素的化合价是+2,氯元素的化合价是-1,氯化镁的化学式是MgCl2.故填:MgCl2;
(2)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以氯化镁中氯元素的化合价为-1价,可表示为
.故填:
;
(3)该物质由镁离子和氯离子构成,镁离子为阳离子,表示为:Mg2+;
(4)金属镁和稀盐酸反应,生成物为氯化镁和氢气,其反应方程式为:Mg+2HCl=MgCl2+H2↑.故填:Mg+2HCl=MgCl2+H2↑.
(2)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以氯化镁中氯元素的化合价为-1价,可表示为
| -1 |
| Cl |
| -1 |
| Cl |
(3)该物质由镁离子和氯离子构成,镁离子为阳离子,表示为:Mg2+;
(4)金属镁和稀盐酸反应,生成物为氯化镁和氢气,其反应方程式为:Mg+2HCl=MgCl2+H2↑.故填:Mg+2HCl=MgCl2+H2↑.
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学反应方程式的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2表示.

【探究一】
碱式碳酸镁的制备碱式碳酸镁可用MgCO3和(NH4)2CO3
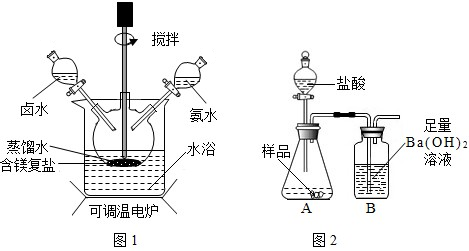
作原料制备.取一定量的原料放入三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图所示),加入一定量蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达40℃时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10分钟,一段时间后过滤洗涤,滤出的固体在120℃干燥得到碱式碳酸镁产品.回答下列问题:
(1)①搅拌的目的是______;②选择水浴加热方式,其优点是______.
(2)所得碱式碳酸镁产品中常检出有少量Cl-,其原因是混有______(填化学式).
(3)图1设计实验检验碱式碳酸镁中含有Cl-
| 实 验 操 作 | 实验现象 | 实验结论 |
| ①取样溶解,向样品溶液中滴加过量稀硝酸. ②再向上述所得溶液加______溶液 | 现象①______; 现象②______; | 含有Cl- |
现利用图2所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀质量,以确定碱式碳酸镁中MgCO3的质量分数.请回答下列问题.
(1)若测定值比实际值小,可能的原因有______.(填序号)
①装置A中水蒸气、HCl等进入装置B中
②装置A中CO2未完全进入装置B
③CO2气流速度太快导致Ba(OH)2未完全吸收
④盐酸未滴加过量
(2)为减少误差,现采取一些措施:为防止HCl进入B装置,可在A、B之间增加装有______(填药品名称或化学式)溶液的洗气瓶;将装置B中的长导管下方增加一个带孔球泡,可以提高______;在装置B的后面再增加一个装有______(填药品名称或化学式)的干燥管.
(3)准确称取8.00g样品三份,进行测定,测得BaCO3平均质量为3.94g.试计算样品中MgCO3的质量分数(写出计算过程).