题目内容
2.化学是一门以实验为基础的学科,根据图,回答问题.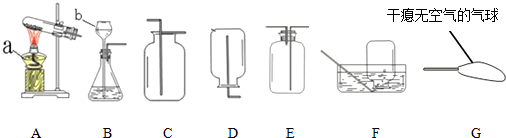
(1)仪器a的名称是酒精灯,仪器b的名称是长颈漏斗
(2)实验室用过氧化氢和二氧化锰制取氧气,选用的发生装置是B(填字母序号),其中二氧化锰起催化作用.写出该反应的符号表达式2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑该反应属于什么基本反应类型分解反应.
(3)某同学欲用高锰酸钾制氧气,并完成铁丝在氧气中燃烧的实验,他应选择A和F的组合来制取氧气,其中A装置中试管口部的棉花的作用是防止加热时高锰酸钾粉末进入导管,写出高锰酸钾制氧气的符号表达式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3).常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.某同学欲收集一瓶氨气可选择上图中的哪些装置收集EG.
分析 (1)据常用仪器回答;
(2)过氧化氢和二氧化锰制取氧气,属于固液常温型,故选发生装置B,二氧化锰在反应中起催化作用,据反应原理书写符号表达式,据反应特点判断反应类型;
(3)做铁丝燃烧实验集气瓶底要放一些水,所以最好用排水法收集,A装置中试管口放棉花是为了防止加热时高锰酸钾粉末进入导管,据反应原理书写符号表达式;
(4)氨气密度比空气小,极易溶于水,所以不能用排水法收集,有刺激性气味,所以要进行尾气处理,据此解答.
解答 解:(1)标号仪器分别是酒精灯和长颈漏斗;
(2)过氧化氢和二氧化锰制取氧气,属于固液常温型,故选发生装置B,二氧化锰在反应中起催化作用,反应的符号表达式为:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应由一种物质生成两种物质,属于分解反应;
(3)做铁丝燃烧实验集气瓶底要放一些水,所以最好用排水法收集,A装置中试管口放棉花是为了防止加热时高锰酸钾粉末进入导管,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应的符号表达式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)氨气密度比空气小,极易溶于水,所以不能用排水法收集,有刺激性气味,所以可用气球将尾气收集起来进行尾气处理;
故答案为:(1)酒精灯;长颈漏斗;
(2)B;催化;2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;分解反应;
(3)F;防止加热时高锰酸钾粉末进入导管;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)EG.
点评 本题综合考查了学生的基本实验能力,涉及仪器的用途、符号表达式的书写、装置选择、实验注意事项等知识,只有掌握相关并理解相关化学知识才能够正确的解答.

 名校课堂系列答案
名校课堂系列答案【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验一 | 实验二 | 实验三 | |
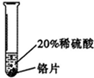 | 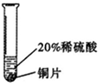 | 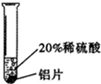 | |
| 实验现象 | 铬片表面产生气泡缓慢,溶液变蓝色 | 无现象 | 铝片表面产生气泡较快 |
| 实验结论 | 铬能和稀硫酸发生反应,反应速率较慢 | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中由强到弱的相对位置关系是Al、Cr、Cu | |||
(1)用砂纸打磨金属片的目的是除去金属表面氧化物
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是无法比较铬和铝的金属活动性强弱
(4)小东思考后认为用铝片、铬片和硫酸铜溶液三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,你能写出小东设想的实验方案吗?请简要的写出实验步骤、实验现象和结论
| 实验步骤 | 实验现象 | 实验结论 |
| A. | 碳元素 | B. | 碳原子 | C. | 碳单质 | D. | 二氧化碳 |
 ”表示氧原子,“〇”表示氢原子).
”表示氧原子,“〇”表示氢原子).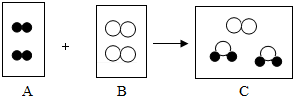
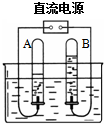 (1)如图是电解水的装置,通电一段时间后,B试管中收集到的气体是氧气,A试管和B试管中收集到的气体的体积比约等于2:1.此反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(1)如图是电解水的装置,通电一段时间后,B试管中收集到的气体是氧气,A试管和B试管中收集到的气体的体积比约等于2:1.此反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑; ”.资料上这个化学方程式中最后一种物质的化学式印刷不清楚,请推测其化学式:H2SO4.在上教版九年级化学教材中即用此原理检验含硫火柴中的硫元素.
”.资料上这个化学方程式中最后一种物质的化学式印刷不清楚,请推测其化学式:H2SO4.在上教版九年级化学教材中即用此原理检验含硫火柴中的硫元素.