题目内容
12.下列物质的用途主要是由其化学性质决定的是( )| A. | 干冰可用于人工降雨 | B. | 活性炭可用于除去冰箱中的异味 | ||
| C. | 铜丝可用作导线 | D. | 硫酸可用于金属除锈 |
分析 物质在化学变化中表现出来的性质叫化学性质,物质不需要发生化学变化就表现出来的性质,叫物理性质;物理性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、导热性、溶解性、挥发性等.干冰升华吸热,可用于人工降雨、做制冷剂等,不属于化学性质;活性炭具有吸附性,可用于除去冰箱中的异味,吸附性属于物理性质;铜丝可用作导线,是利用铜的导电性,属于物理性质;硫酸可用于金属除锈生成新物质,属于硫酸的化学性质.
解答 解:A、干冰升华吸热,可用于人工降雨、做制冷剂等,不属于化学性质,故选项错误;
B、活性炭具有吸附性,可用于除去冰箱中的异味,吸附性属于物理性质,故选项错误;
C、铜丝可用作导线,是利用铜的导电性,属于物理性质,故选项错误;
D、硫酸可用于金属除锈生成新物质,属于硫酸的化学性质,故选项正确;
故选D
点评 本考点考查了物理性质和化学性质的区分,要记忆有关二氧化碳、活性炭、铜丝和硫酸的性质,并能够在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
2.下列除去杂质(括号内)的方法正确的是( )
| A. | CO(CO2):通过灼热的氧化铜 | B. | NaCl溶液(盐酸):加热蒸发 | ||
| C. | NaOH溶液(Na2CO3):加适量稀盐酸 | D. | 铁粉(氧化铜粉末):加入足量稀硫酸 |
3.柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业.如图2、3是两种不同方法制备一水柠檬酸晶体(C6H8O7•H2O)的工艺流程图.回答相关问题:
【资料卡片】: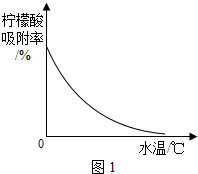
①柠檬酸水溶液显酸性,柠檬酸钙不溶于水;
②工业生产柠檬酸,原料预处理后,得到的发酵液中含有柠檬酸及其他可溶性杂质;
③一水柠檬酸在不同温度下的溶解度如下表:
④某种专用树脂对柠檬酸的吸附率和水温的关系如图1:
【钙盐法制备】(图2)
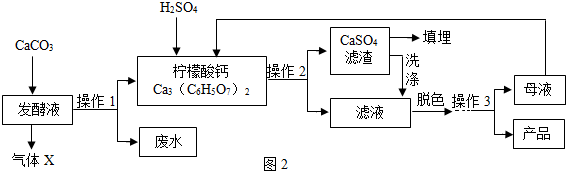
(1)实验室检验气体X时发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;
(2)操作3的目的是得到一水柠檬酸晶体,操作顺序是加热浓缩→冷却结晶→过滤.
(3)洗涤CaSO4滤渣的目的是提高产量;
(4)母液可以循环,其中一定含有的溶质是柠檬酸;
【变温色谱分离法制备】(图3)
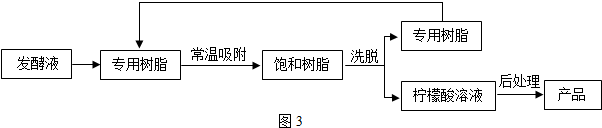
(5)洗脱的目的是使专用树脂再生,洗脱时在较高温度下的热水进行,其原因是专用树脂对柠檬酸的吸附率随温度升高而降低,温度越高,越便于柠檬酸从专用树脂中分离;
(6)对比“变温色谱分离法”,请你说出“钙盐法”的劣势钙盐法中增加了废水及CaSO4滤渣后期处理的费用;增加了CO2的排放;消耗资源,破坏环境.
【资料卡片】:

①柠檬酸水溶液显酸性,柠檬酸钙不溶于水;
②工业生产柠檬酸,原料预处理后,得到的发酵液中含有柠檬酸及其他可溶性杂质;
③一水柠檬酸在不同温度下的溶解度如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | … |
| 溶解度/g | 96 | 118 | 146 | 183 | 216 | … |
【钙盐法制备】(图2)

(1)实验室检验气体X时发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;
(2)操作3的目的是得到一水柠檬酸晶体,操作顺序是加热浓缩→冷却结晶→过滤.
(3)洗涤CaSO4滤渣的目的是提高产量;
(4)母液可以循环,其中一定含有的溶质是柠檬酸;
【变温色谱分离法制备】(图3)

(5)洗脱的目的是使专用树脂再生,洗脱时在较高温度下的热水进行,其原因是专用树脂对柠檬酸的吸附率随温度升高而降低,温度越高,越便于柠檬酸从专用树脂中分离;
(6)对比“变温色谱分离法”,请你说出“钙盐法”的劣势钙盐法中增加了废水及CaSO4滤渣后期处理的费用;增加了CO2的排放;消耗资源,破坏环境.
20.生活中的食醋(含醋酸)除作调味剂外,还有很多用途.下列不属于食醋用途的是( )
| A. | 鉴别黄金饰品中是否含有铜 | B. | 除去菜刀上的铁锈 | ||
| C. | 清洗溅到皮肤上的碱液 | D. | 除去水壶壁上的水垢 |
7. 某品牌碳酸氢铵化肥的标签如下图所示.根据相关信息判断下列计算正确的是( )
某品牌碳酸氢铵化肥的标签如下图所示.根据相关信息判断下列计算正确的是( )
 某品牌碳酸氢铵化肥的标签如下图所示.根据相关信息判断下列计算正确的是( )
某品牌碳酸氢铵化肥的标签如下图所示.根据相关信息判断下列计算正确的是( )| A. | 碳酸氢铵中氮、氢、氧、碳四种元素的质量比14:4:12:48 | |
| B. | 碳酸氢铵中各元素的质量分数由大到小的顺序为O、C、H、N | |
| C. | 该化肥中碳酸氢铵的纯度为79% | |
| D. | 每袋该化肥中含氮量与30kg尿素[化学式为CO(NH2)2]含氮量相当 |
1.下列4个图象能正确反映对应变化关系是( )
| A. | 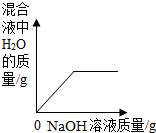 向一定量稀H2SO4中加入NaOH溶液 向一定量稀H2SO4中加入NaOH溶液 | |
| B. | 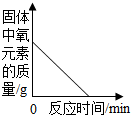 用酒精灯加热一定量KMnO4固体 用酒精灯加热一定量KMnO4固体 | |
| C. | 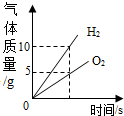 将水通电电解一段时间 将水通电电解一段时间 | |
| D. | 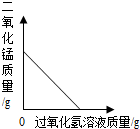 向一定量的二氧化锰中加入H2O2溶液 向一定量的二氧化锰中加入H2O2溶液 |
11.请根据如图所示的实验装置图填空.
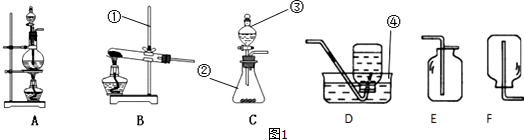
(1)指出图1中标有数字的仪器的名称:①铁架台,②锥形瓶,③分液漏斗,④水槽.
(2)在实验室用高锰酸钾制氧气时应该选择的发生装置是B,装置中还缺少一种实验用品棉花,其作用是防止固体进入导管.写出反应的文字(或符号)表达式:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气(或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑).
(3)当用C装置制取氧气时,仪器③内盛放的液体是过氧化氢溶液,反应文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(4)在实验室制取并收集二氧化碳可选用CE 装置(填字母编号),写出实验室制取二氧化碳反应的文字表达式:碳酸钙+盐酸→氯化钙+水+二氧化碳.验证二氧化碳收集满的方法是燃着的木条放在集气瓶口.
(5)氢气是一种密度比空气小的气体,难溶于水.实验室常用金属锌粒和稀硫酸在常温下反应来制取氢气.实验室制取氢气的发生装置可以选择上图中的C装置,收集氢气可以选择上图中的D或F装置.
(6)实验室用加热二氧化锰和浓盐酸混合物的方法制取氯气,应该选择的发生装置是A.
(7)图2所示装置也可以用来收集气体.如果用该装置收集二氧化碳,气体应该从A导管通入.如果用排水法收集氧气,应该先在该装置中装满水,然后将氧气从B导管通入.
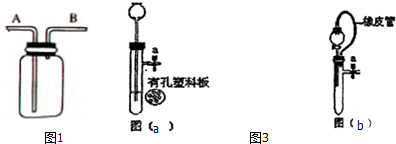
(8)小宋同学对气体发生装置作了改进,设计了如图3的装置,如图3(a)所示.使用图3(a)装置制取CO2,反应进行过程中,关闭该装置中的止水夹a后,可以观察到的现象液体被压回长颈漏斗中,固液分离,反应停止.
(9)小亮同学也改进了气体发生装置,改进的装置如图3(b)所示,与C装置相比较,橡皮管的作用是平衡气压或使分液漏斗和试管中的压强一致,便于液体滴落下来.
(10)小明同学探究了影响双氧水分解速度的某种因素.实验数据记录如下:
实验结论:在相同条件下,双氧水的浓度越大,双氧水分解得越快.

(1)指出图1中标有数字的仪器的名称:①铁架台,②锥形瓶,③分液漏斗,④水槽.
(2)在实验室用高锰酸钾制氧气时应该选择的发生装置是B,装置中还缺少一种实验用品棉花,其作用是防止固体进入导管.写出反应的文字(或符号)表达式:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气(或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑).
(3)当用C装置制取氧气时,仪器③内盛放的液体是过氧化氢溶液,反应文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(4)在实验室制取并收集二氧化碳可选用CE 装置(填字母编号),写出实验室制取二氧化碳反应的文字表达式:碳酸钙+盐酸→氯化钙+水+二氧化碳.验证二氧化碳收集满的方法是燃着的木条放在集气瓶口.
(5)氢气是一种密度比空气小的气体,难溶于水.实验室常用金属锌粒和稀硫酸在常温下反应来制取氢气.实验室制取氢气的发生装置可以选择上图中的C装置,收集氢气可以选择上图中的D或F装置.
(6)实验室用加热二氧化锰和浓盐酸混合物的方法制取氯气,应该选择的发生装置是A.
(7)图2所示装置也可以用来收集气体.如果用该装置收集二氧化碳,气体应该从A导管通入.如果用排水法收集氧气,应该先在该装置中装满水,然后将氧气从B导管通入.

(8)小宋同学对气体发生装置作了改进,设计了如图3的装置,如图3(a)所示.使用图3(a)装置制取CO2,反应进行过程中,关闭该装置中的止水夹a后,可以观察到的现象液体被压回长颈漏斗中,固液分离,反应停止.
(9)小亮同学也改进了气体发生装置,改进的装置如图3(b)所示,与C装置相比较,橡皮管的作用是平衡气压或使分液漏斗和试管中的压强一致,便于液体滴落下来.
(10)小明同学探究了影响双氧水分解速度的某种因素.实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MmO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |