题目内容
取13.8 g R2CO3(R为未知金属元素)固体完全溶于水得到100 g溶液,加人一定质量溶质质量分数为34.2%的Ba(OH)2溶液,恰好完全反应,过滤,得到BaCO3沉淀19.7 g.向所得的滤液中滴入酚酞试液,溶液变红,逐滴加入20 g一定溶质质量分数的稀盐酸,溶液刚好变成无色.试计算:
(1)R的相对原子质量;
(2)所加Ba(OH)2溶液的质量;
(3)最后所得RCl溶液的溶质质量分数(计算结果保留一位小数).
解析:
|
(1)解:设R的相对原子质量为x,生成ROH的质量为y,氢氧化钡溶液的质量为z R2CO3+Ba(OH)2=BaCO3↓+2ROH 60+2x 171 197 2x+34 13.8 g 34.2%z 19.7 g (60+2x):13.8 g=197:19.7 g=(2x+34)∶y=171∶34.2%z x=39 y=11.2 g z=50 g R的相对原子质量为39 (2)Ba(OH)2溶液的质量为50 g (3)设ROH与HC1反应生成RCl的质量为m ROH+HCl=RC1+H2O 56 74.5 11.2 g m 56∶11.2 g=74.5∶m m=14.9 g 溶液中溶质的质量分数为[14.9 g/(100+50+20-19.7)g]×100%=9.9% (每小题2分,共6分)(计算过程中未代入单位,不扣分;每小题关系式1分,结果1分) |

 智慧小复习系列答案
智慧小复习系列答案 某钙片的标签如右,且知此钙片成分中只有碳酸钙含有钙元素:
某钙片的标签如右,且知此钙片成分中只有碳酸钙含有钙元素:
(1)请通过计算说明此标签中的含钙量是错误的.
(2)为测定其真实的含钙量,小东每次取10片钙片放入已称量的含足量盐酸的烧杯中,发生的化学反应是:CaCO3+2HCl═CaCl2+H2O+CO2↑,充分反应后再称取烧杯和剩余物的总质量,小东做了三次实验,数据如下
| 物质的质量 | 第一次 | 第二次 | 第三次 | 平均值 |
| 反应前:烧杯+盐酸 | 22 g | 22 g | 22 g | 22 g |
| 10片钙片 | 8 g | 8 g | 8 g | 8 g |
| 反应后:烧杯十剩余物 | 26.7 g | 26.5 g | 26.9 g | 26.7g |
②请列式计算每片此钙片的含钙量,并建议厂家如何修改标签.
碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域。为测定碳酸镁晶须中n的值,学习小组设计了如下装置并进行了3次实验:(不考虑稀盐酸挥发)
【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;
b、相对分子质量:[Mr(MgCO3)∶84、Mr(H2O)∶18、Mr(MgO)∶40、Mr(CO2)∶44]
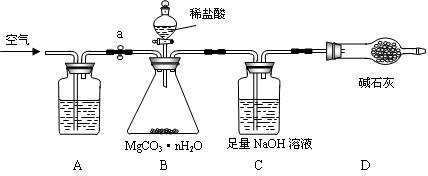
【实验步骤】
① ▲ ;
②准确称取3.45g MgCO3·nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体为止;
⑤打开弹簧夹a, ▲ ;
| 编 号 | 1 | 2 | 3 |
| 实验前 | 228.00 | 228.00 | 228.00 |
| 实验后 | 229.10 | 229.11 | 229.09 |
⑥准确称量C装置的质量(如右表);
⑦重复上述步骤;
⑧根据数据进行计算。
【实验分析及数据处理】
(1)完善实验步骤:① ▲ ;⑤ ▲ ;
(2)请计算碳酸镁晶须中的n值。(要求有计算过程,3分)
(3)A装置中盛放的溶液是 ▲ ;
(4)D装置的作用是 ▲ ;
【实验反思】
(5)实验结果与理论值有偏差,原因可能是 ▲ ;
(6)下列选项中,会造成实验结果偏大的是 ▲ ;偏小的是 ▲ ;
①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
⑤稀盐酸滴加速率太快; ⑥C装置中NaOH溶液浓度过大;
(7)为精确测定n的值,在老师指导下,小组同学称取13.8 g MgCO3·nH2O进行热重分析,并绘制出如图所示的热重曲线示意图。则:
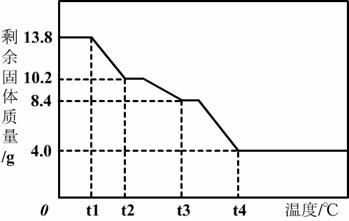
①t2℃时,剩余固体为 ▲ (填化学式);
②最终剩余的4.0 g物质是 ▲ (填化学式);
③MgCO3·nH2O完全分解的化学方程式为: ▲ 。