题目内容
3.A~H都是初中化学常见物质.其中A、B的组成元素相同,且常温下都是无色液体;H是蓝色沉淀.X、Y都是氧化物,其中X是黑色粉末状固体,Y常用作食品干燥剂,Z是红色固体.它们之间有如图转化关系.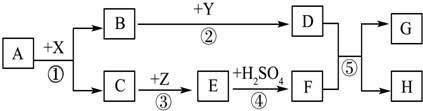
根据上述信息,回答下列问题:
(1)反应①中X起催化作用.
(2)反应②的化学方程式CaO+H2O=Ca(OH)2.
(3)反应⑤的化学方程式CuSO4+Ca(OH)2=CaSO4+Cu(OH)2↓.
(4)此转化关系中没有涉及到的基本反应类型是置换反应.
分析 根据A-H都是初中化学常见物质,Y常用作食品干燥剂,所以Y是氧化钙,A、B的组成元素相同,且常温下都是无色液体,X是黑色粉末状固体,氧化钙会与B反应是B是水,A是过氧化氢溶液,过氧化氢分解生成水和氧气,所以C是氧气,X是二氧化锰,Z是红色固体,所以Z是铜,E是氧化铜,氧化铜和硫酸反应生成硫酸铜和水,所以F是硫酸铜,氧化钙和水反应生成氢氧化钙,所以D是氢氧化钙,氢氧化钙和硫酸铜反应生成硫酸钙和氢氧化铜沉淀,H是蓝色沉淀,所以H是氢氧化铜,G是硫酸钠,然后将推出的物质进行验证即可.
解答 解:(1)A-H都是初中化学常见物质,Y常用作食品干燥剂,所以Y是氧化钙,A、B的组成元素相同,且常温下都是无色液体,X是黑色粉末状固体,氧化钙会与B反应是B是水,A是过氧化氢溶液,过氧化氢分解生成水和氧气,所以C是氧气,X是二氧化锰,Z是红色固体,所以Z是铜,E是氧化铜,氧化铜和硫酸反应生成硫酸铜和水,所以F是硫酸铜,氧化钙和水反应生成氢氧化钙,所以D是氢氧化钙,氢氧化钙和硫酸铜反应生成硫酸钙和氢氧化铜沉淀,H是蓝色沉淀,所以H是氢氧化铜,G是硫酸钠,经过验证,推导正确,所以X是二氧化锰,起催化作用;
(2)反应②是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(3)反应⑤是氢氧化钙和硫酸铜反应生成硫酸钙和氢氧化铜沉淀,化学方程式为:CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4;
(4)过氧化氢生成氧气的反应属于分解反应,氧化钙和水生成氢氧化钙的反应属于化合反应,氢氧化钙和硫酸铜生成氢氧化铜沉淀的反应属于复分解反应,所以没有涉及到的基本反应类型是置换反应.
故答案为:(1)催化;
(2)CaO+H2O=Ca(OH)2;
(3)CuSO4+Ca(OH)2=CaSO4+Cu(OH)2↓;
(4)置换.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | 氧气的化学性质比较活泼,属于可燃物 | |
| B. | 氮气的化学性质不活泼,常用作保护气 | |
| C. | 稀有气体在通电时发出不同颜色的光,发生了化学变化 | |
| D. | 二氧化碳在空气中含量增多会使温室效应加剧,属于空气污染物 |
| A. | 活性炭吸附冰箱内的异味 | B. | 浓盐酸的挥发 | ||
| C. | 植物的光合作用 | D. | 积沙成塔 |
| A. | CO(NH2)2 | B. | KNO3 | C. | Ca(H2PO4)2 | D. | KCl |
| A. | 二氧化碳用来灭火 | B. | 生石灰用作食品包装袋中的干燥剂 | ||
| C. | 盐酸用于除锈 | D. | 干冰用来人工降雨 |
 实验室发现一只久置且标签破损的试剂瓶,老师说可能是氢氧化钠、碳酸钠、氢氧化钙、氯化钠和氯化钙等五种溶液中的一种.请通过探究实验,确定其成分:
实验室发现一只久置且标签破损的试剂瓶,老师说可能是氢氧化钠、碳酸钠、氢氧化钙、氯化钠和氯化钙等五种溶液中的一种.请通过探究实验,确定其成分:【查询资料】
①氢氧化钙为微溶于水,其他物质为易溶于水
②氯化钠和氯化钙溶液为中性,其他物质的溶液为碱性溶解度的相对大小(20℃)
| 溶解度/g | 一般称为 |
| <0.01 | 难溶 |
| 0.01-1 | 微溶 |
| 1-10 | 可溶 |
| >10 | 易溶 |
(2)向样品溶液中加入酚酞试剂呈红色,则一定不可能是NaCl、CaCl2(填化学式);
(3)将上述液体分成三等份,甲、乙、丙同学继续完成实验:
| 实验步骤 | 实验现象 | 实验结论 | |
| 甲 | 加入过量的稀盐酸 | 产生气体,溶液为无色 | Na2CO3 |
| 乙 | 加入过量的澄清石灰水 | 产生沉淀,溶液为红色 | Na2CO3 |
| 丙 | 加入过量的CaCl2溶液 | 产生沉淀,溶液为红色 | Na2CO3和NaOH |
根据该实验结论判断原药品已变质,则原药品在空气中久置变质的反应的化学方程式为2NaOH+CO2═Na2CO3+H2O;
(4)实验结束,将三位同学反应后的物质全部都倒入废液缸中,发现出现白色固体且上层溶液呈无色,则溶液中一定含有的溶质是BE(填序号).
A.NaOH B.NaCl C.HCl
D.Na2CO3 E.CaCl2 F.Ca(OH)2.
