题目内容
12.某保健品主要成分为碳酸钙化学式为CaCO3 请完成下列问题:(1)其含有三种元素,一个分子由5个原子构成,其相对分子质量为100.
(2)碳酸钙中钙元素的质量分数是多少?(写出计算过程)
(3)某儿童现需要补充钙元素200mg,则该儿童需食用该钙片(指碳酸钙)多少g?(写出计算过程)
分析 (1)根据碳酸钙化学式的含义、相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,分析解答;
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)碳酸钙是由钙、碳、氧三种元素组成的;一个碳酸钙分子中含有1个钙原子、1个碳原子和3个氧原子,共5个原子;其相对分子质量为40+12×3+16×3=100.
故填:三;5;100;
(2)碳酸钙中钙元素的质量分数是$\frac{40}{100}$×100%=40%;故填:40%;
(3)某儿童现需要补充钙元素200mg,则该儿童应食用该钙片(指碳酸钙)的质量为200mg÷40%=500mg=0.5g;故填:0.5g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
7.下列化学现象的描述,正确的是( )
| A. | 把盛有红磷的燃烧匙伸人氧气集气瓶中,磷立即燃烧 | |
| B. | 铁丝在氧气中燃烧,火星四射,生成一种白色固体 | |
| C. | 木炭在氧气中燃烧比在空气中燃烧旺,发出白光 | |
| D. | 硫在氧气中燃烧生成一种白色固体 |
4.氢化钙(CaH2)是一种储氢材料,是登山运动员常用的能源提供剂.甲、乙两位同学选用如图装置(固定装置省略),用氢气与金属钙加热制备氢化钙.实验结束后,两位同学对硬质玻璃管中的固体进行如下探究:
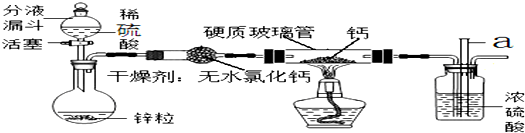
【提出问题】硬质玻璃管中的钙是否完全转化为CaH2?
【查阅资料】
(1)金属钙活动性很强,遇水反应生成氢化钙,同时产生一种气体;
(2)氢化钙要密封保存,遇水反应放出氢气.
【猜想与实验】
(1)固体为Ca和CaH2.
(2)固体为CaH2.
甲同学的探究活动如下:
【实验反思】
乙同学认为由以上探究活动还不能得出猜想1正确,理由是若固体为CaH2,遇水反应也会产生相同的现象,请你帮助乙设计实验,写出主要的实验步骤、现象和相应结论:取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH2;若不相等,则说明Ca未完全转化为CaH2.
【反思讨论】
(1)写出CaH2与水反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是便于携带、避免爆炸危险.
(3)制备CaH2装置中,玻璃管a的作用是检验装置的气密性.

【提出问题】硬质玻璃管中的钙是否完全转化为CaH2?
【查阅资料】
(1)金属钙活动性很强,遇水反应生成氢化钙,同时产生一种气体;
(2)氢化钙要密封保存,遇水反应放出氢气.
【猜想与实验】
(1)固体为Ca和CaH2.
(2)固体为CaH2.
甲同学的探究活动如下:
| 实验操作 | 实验现象 | 实验结论及解释 |
| ①取少量硬质玻璃管中的固体于试管中,滴入少量水,收集产生的气体,并用燃着的木条点燃. | 冒气泡;气体燃烧,产生淡蓝色火焰 | 有氢气生成 |
| ②继续向溶液中滴加酚酞. | 呈红色 | 生成Ca(OH)2(填化学式) |
乙同学认为由以上探究活动还不能得出猜想1正确,理由是若固体为CaH2,遇水反应也会产生相同的现象,请你帮助乙设计实验,写出主要的实验步骤、现象和相应结论:取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH2;若不相等,则说明Ca未完全转化为CaH2.
【反思讨论】
(1)写出CaH2与水反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是便于携带、避免爆炸危险.
(3)制备CaH2装置中,玻璃管a的作用是检验装置的气密性.
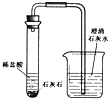 在盛有少量石灰石的试管里加入适量稀盐酸,并将导管的一段伸入装有澄清石灰石的烧杯中,依据实验回答下列问题:
在盛有少量石灰石的试管里加入适量稀盐酸,并将导管的一段伸入装有澄清石灰石的烧杯中,依据实验回答下列问题: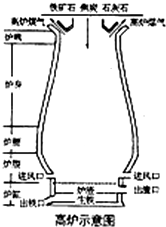 早在春秋战国时期,我国就开始生产和使用铁器.公元1世纪时,铁在我国已经广泛使用.如图为工业炼铁的主要设备--高炉.请你回答下列问题:
早在春秋战国时期,我国就开始生产和使用铁器.公元1世纪时,铁在我国已经广泛使用.如图为工业炼铁的主要设备--高炉.请你回答下列问题: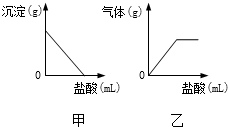 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH 中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如右图甲、乙所示.
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH 中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如右图甲、乙所示.