题目内容
18.伊伐布雷定(C27H36N2O5)是世界上治疗心脏病的最新药物之一.下列有关伊伐布雷定的说法错误的是( )| A. | 伊伐布雷定由 70 个原子构成 | B. | 伊伐布雷定属于有机化合物 | ||
| C. | 伊伐布雷定由 4 种元素组成 | D. | 伊伐布雷定的相对分子质量为 468 |
分析 A.根据分子结构来分析;
B.根据有机物的概念来分析;
C.根据化学式的意义来分析;
D.根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析.
解答 解:A.由化学式C27H36N2O5可知,一个伊伐布雷定分子是由27个碳原子、36个氢原子、2个氮原子和5个氧原子构成的,共70个原子,不能说伊伐布雷定由 70 个原子构成,故错误;
B.由伊伐布雷定的化学式(C27H36N2O5)可知,它是一种含碳元素的化合物,属于有机化合物,故正确;
C.由伊伐布雷定的化学式(C27H36N2O5)可知,它是碳、氢、氮、氧元素四种元素组成的,故错误;
D.由伊伐布雷定的化学式(C27H36N2O5)可知,它的相对分子质量=12×27+1×36+14×2+16×5=468,故正确.
故选A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义、氧化物与化合物的特征进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.甲、乙、丙三种物质在不同温度下的溶解度见下表:
下列有关说法正确的是( )
| 0℃ | 30℃ | 60℃ | 90℃ | |
| 甲 | 13.3克 | 45.8克 | 110克 | 202克 |
| 乙 | 35.5克 | 36.0克 | 37.1克 | 38.1克 |
| 丙 | 0.18克 | 0.16克 | 0.12克 | 0.08克 |
| A. | 降低温度可使丙的不饱和溶液变为饱和溶液 | |
| B. | 甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙 | |
| C. | 0℃时,三种物质的饱和溶液溶质质量分数甲>乙>丙 | |
| D. | 使乙物质从一定温度下的饱和溶液中析出,一般采用蒸发溶剂的方法 |
6.在制取CO2的实验中,小科发现质量相同而粗细不同的大理石与盐酸反应,CO2的产生速度细的比粗的快得多.经思考后,小科设计了如下实验(每次实验均用1g大理石,20mL盐酸)
(1)为了比较反应速度,设计如图一所示装置,其中量筒的作用是通过观察单位时间内排入量筒中水的体积来判断反应速率;
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.
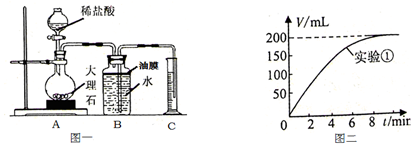
(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?
| 实验序号 | 温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| 1 | 20 | 粗 | 5 | 探究大理石和盐酸的反应速度与石灰石颗粒大小的关系 |
| 2 | 20 | 细 | 5 |
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.

(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?
13.下列关于水资源的叙述,正确的是( )
| A. | 通常所说的水资源是指陆地上的所有水体 | |
| B. | 冰川分布于两极和高山地区,是目前可供人类利用的最重要的水资源之一 | |
| C. | 目前你用的淡水资源,主要是指河流水、湖泊淡水河浅层地下水 | |
| D. | 水资源开发利用后,都能很快恢复 |
3.下列推测、推断或解释、归纳正确的是( )
| A. | 食盐溶液、蔗糖溶液是$\stackrel{推断}{→}$无色的无色的液体都是溶液 | |
| B. | 在室温下的硝酸钾饱和溶液$\stackrel{推测}{→}$此时该溶液不能再溶解其它任何物质了 | |
| C. | 粉末状食盐比粗的颗粒状食盐溶解快$\stackrel{解释}{→}$由于物质的溶解性与颗粒大小有关 | |
| D. | 氢氧化钠溶于水时温度会升高$\stackrel{归纳}{→}$有些物质溶解时会放热 |
10.物质的用途主要由其性质决定.下列物质的用途是利用其化学性质的是( )
| A. | 用氢氧化钠作干燥剂 | B. | 将氮气充入灯泡保护灯丝 | ||
| C. | 用活性炭消除房间的异味 | D. | 用干冰营造仙境般的舞台效果 |
7.A在B中充分燃烧生成C和D,A、B、C、D的微观示意图如图表所示.
看图回答:
(1)A中氮、氢原子数之比为1:3,氮、氢元素质量比为14:3.
(2)A在B中充分燃烧的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2,基本反应类型为置换反应.
| 物质 | A | B | C | D | 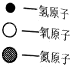 |
| 分子示意图 |  | 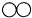 |  |  |
(1)A中氮、氢原子数之比为1:3,氮、氢元素质量比为14:3.
(2)A在B中充分燃烧的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2,基本反应类型为置换反应.
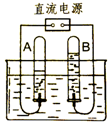 水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.
水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.