题目内容
13.日本核电站泄漏事故备受关注,在浙江有谣言称食用碘盐可以防核辐射,引发宁波等一些地方出现碘盐抢购现象,专家认为谣言荒谬,抢购碘盐毫无必要为了消除碘缺乏病,我国政府规定某些地区居民的食用盐中必须加碘.如图为江西某盐业总公司生产的加碘盐部分标签,请根据图中标签回答问题:
(1)碘酸钾(KIO3)中碘元素的化合价为+5.
(2)从“食用方法”推测,碘酸钾(KIO3)的一种化学性质是_受热易分解(或不稳定).
(3)已知成人每天约需0.15mg碘,假设这些碘主要是从碘盐中摄取的.若1000g碘盐中含20mg碘,则成人每天需食用这种碘盐7.5g.
分析 (1)化合物中,元素化合价代数和为零;
(2)根据储存方法和食用方法进行分析解答;
(3)根据混合物中元素的含量,由元素质量计算混合物的质量.
解答 解:(1)设碘酸钾中碘元素的化合价为x,碘酸钾中,钾元素化合价是+1,氧元素化合价是-2,根据化合物中元素化合价代数和为零有:(+1)+x+(-2)×3=0,x=+5,
故填:+5;
(2)根据储存方法和食用方法,可知:碘酸钾的一种化学性质是受热易分解(不稳定);故答案为:受热易分解(或不稳定);
(3)由题意可知每1000g碘盐中约含20mg碘,则0.15mg碘需碘盐的质量为1000g×$\frac{0.15mg}{20mg}$=7.5g;故填:7.5.
点评 根据化学式的基本计算,结合实际生活进行计算,体验化学的学以致用.

练习册系列答案
相关题目
19.甲、乙两种物质的溶解度曲线如图所示,下列叙述正确的是( )
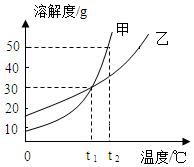

| A. | t1℃时,甲和乙溶液中溶质的质量分数一定相等 | |
| B. | 将甲、乙饱和溶液从t2℃降到t1℃,析出甲的质量大 | |
| C. | 将甲、乙饱和溶液从t1℃升温至t2℃,甲溶液中溶质质量分数比乙大 | |
| D. | t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等 |
20.只用一种试剂(括号内的物质),不能将组内的物质鉴别出来的是( )
| A. | Ca(OH)2、NaCl、Na2SO4、H2SO4四种溶液(碳酸钠溶液) | |
| B. | CuO、Fe、C、Al四种固体粉末(稀硫酸) | |
| C. | NH4NO3、NaOH、CaO、Na2CO3四种白色固体(水) | |
| D. | CO2、O2、H2、空气四种无色气体(燃着的木条) |
1.如图所示的微观变化与下列反应及反应类型对应正确的是( )
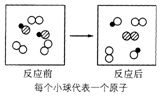

| A. | 2CO+O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2 化合反应 | |
| B. | 2HI+Cl2═2HCl+I2 置换反应 | |
| C. | 2H2O $\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ 分解反应 | |
| D. | 2HCl+CuO═CuCl2+H2O 复分解反应 |
8.M是一种活动性比铁强的金属,M离子(M2+)与其他几种离子构成的化合物的溶解性见下表:
有下列各组物质:①M+HCl ②M(NO3)2+BaCl2 ③MO+HCl ④M(OH)2+NaCl ⑤M(OH)2+HCl ⑥M(NO3)2+HCl ⑦MCO3+HCl ⑧MSO4+BaCl2
其中不能直接反应制取MCl2的是②④⑥.
| O2- | OH- | CO32- | Cl- | SO42- | NO3- | |
| M2+ | 难溶 | 难溶 | 难溶 | 易溶 | 易溶 | 易溶 |
其中不能直接反应制取MCl2的是②④⑥.
18.某市有一家工厂处理含铜垃圾的生产流程如下,下列有关说法正确的是( )


| A. | 步骤①用灼烧法是因为铜能在空气中燃烧 | |
| B. | 步骤②反应后所得的蓝色溶液不可能呈酸性 | |
| C. | ③和⑤两步骤中均有过滤操作 | |
| D. | 步骤④发生的反应类型是复分解反应 |
2.下列对燃烧现象的描述,错误的是( )
| A. | 红磷在空气中燃烧,产生大量的白烟 | |
| B. | 木炭在氧气中燃烧,产生白光,放出二氧化碳气体 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 镁带在空气中燃烧发出耀眼的白光,生成白色固体 |
 将等质量的锌粉和铁粉分别于溶质质量分数相同且等质量的稀硫酸充分反应,产生氢气的质量与时间的关系如图所示.请回答下列问题:
将等质量的锌粉和铁粉分别于溶质质量分数相同且等质量的稀硫酸充分反应,产生氢气的质量与时间的关系如图所示.请回答下列问题: