题目内容
4.请根据下列装置和仪器的示意图,回答下列问题:
(1)写出图中标示仪器的名称:①酒精灯,②集气瓶.
(2)用过氧化氢溶液和二氧化锰制氧气,选择C装置的优点是可以随时添加液体药品或可以控制反应速率,写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;反应结束后,若要过滤分离出MnO2,除了上图所示仪器外,还需补充的玻璃仪器名称是漏斗.
(3)装置E用排空气法收集氢气,则气体应从b(填“a”和“b”)端通入;若要收集干燥的二氧化碳,则E装置中可以盛浓硫酸作干燥剂.
(4)取3.16g高锰酸钾加热一段时间后,测出固体剩余物中钾和氧的原子个数比为1:3,则加热过程中产生氧气的质量为0.32g.
分析 (1)依据实验室常用仪器的认识解决此题;
(2)根据不同的实验装置,功能不同解答;依据用双氧水和二氧化锰制取氧气属于固液常温型选择发生装置,根据质量守恒定律写化学方程式;根据过滤所用的仪器解答;
(3)用排水法收集气体,因为气体的密度都小于液体的密度,必需短进长出;根据浓硫酸具有吸水性可以做干燥剂解答;
(4)根据质量守恒定律,利用反应前后钾元素的质量不变分析解答.
解答 解:(1)依据实验室常用仪器可知酒精灯,集气瓶;
(2)发生装置B或C的优点是:可以随时添加液体药品或可以控制反应速率.
用双氧水和二氧化锰制取氧气属于固液常温型,发生装置为B,根据质量守恒定律写化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;反应结束后,若要过滤分离出MnO2,除了上图所示仪器外,还需补充的玻璃仪器名称是烧杯、玻璃棒、漏斗;
(3)F装置用排水法收集气体为气体的密度都小于液体的密度,必需短进长出,故b进;浓硫酸具有吸水性可以做干燥剂,若要收集干燥的二氧化碳,则E装置中可以盛浓硫酸作干燥剂;
(4)设反应后氧元素的质量为x,
3.16g高锰酸钾中,钾元素的质量为:3.16g×$\frac{39}{158}$=0.78g
氧元素的质量为:3.16g×$\frac{64}{158}$=1.28g
剩余物中钾和氧的原子个数比为1:3时,锰元素和氧元素的质量比为:(39×1):(16×3)=39:48,
反应前后钾元素的质量不变,则有:39:48=0.78g:x,
x=0.96g,
则加热过程中产生氧气的质量为:1.28g-0.96g=0.32g,
答案:
(1)酒精灯; 集气瓶
(2)可以随时添加液体药品或可以控制反应速率 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑; 漏斗;
(3)b;浓硫酸
(4)0.32.
点评 考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案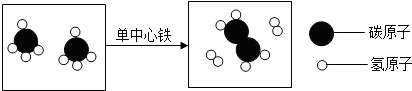
| A. | 反应物和生成物均属于有机物 | |
| B. | “单中心铁”在反应前后质量不变 | |
| C. | “单中心铁”加快了上述反应的速率 | |
| D. | 反应前后原子总数一定没有发生变化 |
| A. | 以粮食为原料酿酒 | B. | 铜制品在潮湿的空气中变成铜绿 | ||
| C. | 气球充气过多爆炸 | D. | 用燃烧法区别羊毛和合成纤维 |
| A. | 下雪后天气变暖,雪融化了 | B. | 潮湿的衣服被晒干了 | ||
| C. | 以粮食为原料酿酒 | D. | 加热,石蜡熔化了 |
| A. |  牛奶 | B. |  瘦肉 | C. |  苹果 | D. |  黄豆 |
| A. | 氯化钠可以配制生理盐水 | B. | 干冰可以用于人工降雨 | ||
| C. | 稀硫酸可以除铁锈 | D. | 氢氧化钠可以作食品干燥剂 |
| A. | 我国古代的“湿法炼铜”:2Fe+3CuSO4═3Cu+Fe2(SO4)3 置换反应 | |
| B. | 实验室用过氧化氢制取氧气:2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑ 分解反应 | |
| C. | 用氢氧化钠溶液吸收二氧化硫:2NaOH+SO2═Na2SO3+H2O 复分解反应 | |
| D. | 新制的生石灰加水能“煮熟”鸡蛋:CaO+H2O═Ca(OH)2 化合反应 |
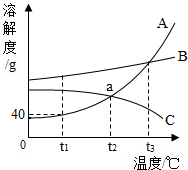 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: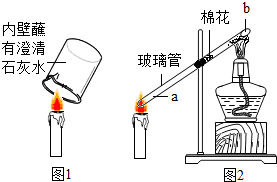 小红做蜡烛燃烧实验时,将内壁沾有澄清石灰水的烧杯罩在蜡烛火焰上(如图1),观察到澄清石灰水变浑浊,化学反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.小芳根据溶解度相关知识提出,该实验不能证明蜡烛燃烧生成了二氧化碳气体,你认为原因是:氢氧化钙的溶解度随温度升高而减小;在不添加实验仪器和药品的情况下(不考虑水分蒸发),请设计一个实验验证蜡烛燃烧生成了二氧化碳气体:将变浑浊的石灰水冷却至室温,浑浊现象没有消失.
小红做蜡烛燃烧实验时,将内壁沾有澄清石灰水的烧杯罩在蜡烛火焰上(如图1),观察到澄清石灰水变浑浊,化学反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.小芳根据溶解度相关知识提出,该实验不能证明蜡烛燃烧生成了二氧化碳气体,你认为原因是:氢氧化钙的溶解度随温度升高而减小;在不添加实验仪器和药品的情况下(不考虑水分蒸发),请设计一个实验验证蜡烛燃烧生成了二氧化碳气体:将变浑浊的石灰水冷却至室温,浑浊现象没有消失.