题目内容
15.氧化铜与氢氧化铜的混合物25.8g,加入稀盐酸恰好完全反应得到325.8g溶液,将滤液结晶得到40.5g的固体.稀盐酸中氢元素的质量分数为( )| A. | 0.2% | B. | 10.3% | C. | 10.5% | D. | 10.6% |
分析 稀盐酸和氧化铜反应生成氯化铜和水,和氢氧化铜反应生成氯化铜和水,根据提供的数据可以进行相关方面的计算和判断.
解答 解:稀盐酸的质量为:325.8g-25.8g=300g,
将滤液结晶得到40.5g的固体,说明反应生成了40.5g氯化铜,
则氯元素质量为:40.5g×$\frac{71}{135}$×100%=21.3g,
因为氯化铜中的氯元素完全来自于稀盐酸,因此稀盐酸中氯元素质量是21.3g,
则稀盐酸中氯化氢质量为:21.3g÷($\frac{35.5}{36.5}$×100%)=21.9g,
氯化氢中氢元素质量为:21.9g-21.3g=0.6g,
稀盐酸中水的质量为:300g-21.9g=278.1g,
水中氢元素质量为:278.1g×$\frac{2}{18}$×100%=30.9g,
稀盐酸中氢元素的质量分数为:$\frac{30.9g+0.6g}{300g}$×100%=10.5%,
故选:C.
点评 本题主要考查学生进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列有关实验现象的描述,正确的是( )
| A. | 镁在空气中燃烧,火星四射 | |
| B. | 红磷在空气中燃烧,产生大量白色烟雾 | |
| C. | 铁钉放入硫酸铜溶液中表面产生红色的铜 | |
| D. | 电解水实验中,正极产生的气体与负极产生的气体体积比为1:2 |
3. “冰城制造”助国产大飞机C919 一飞冲天,中航工业哈飞作为我国首架自主研制的大型客机C919机体结构的制造商主要承担了 4个大部件工作包的制造.下列有关叙述错误的是( )
“冰城制造”助国产大飞机C919 一飞冲天,中航工业哈飞作为我国首架自主研制的大型客机C919机体结构的制造商主要承担了 4个大部件工作包的制造.下列有关叙述错误的是( )
 “冰城制造”助国产大飞机C919 一飞冲天,中航工业哈飞作为我国首架自主研制的大型客机C919机体结构的制造商主要承担了 4个大部件工作包的制造.下列有关叙述错误的是( )
“冰城制造”助国产大飞机C919 一飞冲天,中航工业哈飞作为我国首架自主研制的大型客机C919机体结构的制造商主要承担了 4个大部件工作包的制造.下列有关叙述错误的是( )| A. | 参与国产大飞机制造,有效提升了龙江航空产业制造能力 | |
| B. | 制造客机使用的复合材料主要有机破璃、碳纤维复合材料等 | |
| C. | 制造客机使用的硬铝的主要成分是铝、铜、镁、硅 | |
| D. | 客机使用的燃料航空煤油是石油炼制的产品 |
10. 乙醇俗称酒精,是一种易燃、易挥发的无色液体,能跟水以任意比互溶.医疗上常用体积分数为75%的酒精作消毒剂.下列有关乙醇溶液的说法正确的是( )
乙醇俗称酒精,是一种易燃、易挥发的无色液体,能跟水以任意比互溶.医疗上常用体积分数为75%的酒精作消毒剂.下列有关乙醇溶液的说法正确的是( )
 乙醇俗称酒精,是一种易燃、易挥发的无色液体,能跟水以任意比互溶.医疗上常用体积分数为75%的酒精作消毒剂.下列有关乙醇溶液的说法正确的是( )
乙醇俗称酒精,是一种易燃、易挥发的无色液体,能跟水以任意比互溶.医疗上常用体积分数为75%的酒精作消毒剂.下列有关乙醇溶液的说法正确的是( )| A. | 溶质与溶剂的氢原子个数相等时,溶质与溶剂分子的个数比为1:3 | |
| B. | 乙醇分子中碳元素的质量分数最大 | |
| C. | 乙醇分子的质子与电子的数目不相等 | |
| D. | 乙醇溶液溶质的分子是由碳、氢、氧三种共九个原子组成的 |
20.下列图示的实验操作不正确的是( )
| A. |  过滤 | B. |  检查气密性 检查气密性 | C. |  测溶液pH值 测溶液pH值 | D. |  用滴管取用液体 |
7. 科学家研制一种人造树叶,将水分解成氧和氢,用于生产廉价的环保能源,下列分析错误的是( )
科学家研制一种人造树叶,将水分解成氧和氢,用于生产廉价的环保能源,下列分析错误的是( )
 科学家研制一种人造树叶,将水分解成氧和氢,用于生产廉价的环保能源,下列分析错误的是( )
科学家研制一种人造树叶,将水分解成氧和氢,用于生产廉价的环保能源,下列分析错误的是( )| A. | 人造树叶将水分解成氧和氢是不遵守质量守恒定律的 | |
| B. | 氢是一种优质能源,可作为太空飞船的燃料 | |
| C. | 树叶利用太阳光进行光合作用,将水转变为氢和氧 | |
| D. | 植物光合作用的实质是将光能转变成为化学能 |
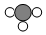
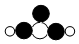
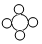
 分别表示H、C、N、O四种原子,下列各项中表示有机物的是( )
分别表示H、C、N、O四种原子,下列各项中表示有机物的是( )