题目内容
9. 如图是甲、乙、丙三种固体的溶解度曲线,试回答:
如图是甲、乙、丙三种固体的溶解度曲线,试回答:①t3°C时,甲、乙、丙三种物质溶解度的大小关系是S甲=S乙>S丙;
②t2°时,20g水最多溶解甲物质10g,其饱和溶液的质量分数为33%;
③t1°C时,在40g水中加入15g丙物质,此时溶液是饱和(填“饱和”或“不饱和”)溶液;
④t3°时,若将50g的甲、乙两种物质分别加入到100g水中,充分溶解后,所得的溶液在溶解度曲线图中可表示为B(“A”、“B”或“C”)点,若将甲溶液降温至t1℃,溶液的变化情况是I、III.
Ⅰ.溶液变为饱和,Ⅱ.溶解度增加,Ⅲ.溶质减少,Ⅳ.溶质的质量分数不变.
分析 (1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)根据已知的温度可以查出有关物质的溶解度;饱和溶液的质量分数=$\frac{溶质的质量}{溶液的质量}$×100%;
(3)根据已知的温度可以查出有关物质的溶解度,从而根据已知条件判断溶液是否饱和;
(4)溶解度曲线的交点表示该温度下两物质的溶解度相等;溶解度曲线下面的点表示溶液不饱和;据溶解度曲线可知物质的溶解度随温度的变化情况,并得到不饱和溶液转化为饱和溶液的方法.
解答 解:(1)观察图示可知:在t3℃时,三种物质的溶解度从大到小的顺序是:S甲=S乙>S丙;
(2)由于在t2℃时,甲物质的溶解度为50g,100克水中最多能溶解50克甲,因此在20克水中最多溶解10克甲,其饱和溶液的质量分数$\frac{10g}{10g+20g}$×100%=33%;
(3)t1°C时,丙的溶解度为30g,100克水中最多能溶解30g丙,故40g水最多可溶解12g丙,故t1°C时,在40g水中加入15g丙物质,此时溶液是饱和溶液;
(4)t3℃时,甲、乙两种物质的溶解度均大于50g,t3℃时,若将50g的甲、乙两种物质分别加入到100g水中,充分溶解后形成不饱和溶液,所得的溶液在溶解度曲线图中可表示为B点;
若将甲溶液降温至t1℃,由图示可知:甲物质的溶解度减至30g,溶液变为饱和,并且有甲物质析出,即溶质减少.
故答案为:(1)S甲=S乙>S丙;(2)10g、33%;(3)饱和;(4)B、I、III.
点评 主要考查了固体的溶解度的理解,根据固体溶解度曲线解决有关的问题,培养学生应用知识的能力

练习册系列答案
相关题目
20.人的机体活动和维持恒定体温需要能量.下列主要为人体提供能量的物质是( )
| A. | 苹果 | B. | 植物油 | C. | 开水 | D. | 食盐 |
17.某农民家中有一种失去标签的化肥可能是碳酸氢铵、氯化铵和硫酸钾的一种.化学兴趣小组为帮他确定该化肥的成分,进行了下列实验.
【反思与评价】:
(1)小凯认为,没有必要进行上述实验也能确定此化肥的种类,他采取的方法为直接闻气味,若有氨味,则为碳酸氢铵.
(2)通过步骤一的实验,请你写出使用铵态氮肥的一点注意事项:不能与碱性物质混合使用.
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取样,加入少量的熟石灰研磨. | 嗅到氨味 | 该化肥一定不是硫酸钾 |
| 步骤二:另取少许样品,加入少量盐酸(或稀硫酸)试剂. | 有大量气泡产生 | 该化肥是碳酸氢铵.发生反应的化学方程式为NH4HCO3+HCl═NH4Cl+H2O+CO2↑ |
(1)小凯认为,没有必要进行上述实验也能确定此化肥的种类,他采取的方法为直接闻气味,若有氨味,则为碳酸氢铵.
(2)通过步骤一的实验,请你写出使用铵态氮肥的一点注意事项:不能与碱性物质混合使用.
18.如图是燃气灶示意图.
(1)如图1是燃气灶的图片:图片中含有的有机合成材料是塑料旋钮.当燃气灶的火焰呈现黄色或橙色,锅底出现黑色,其原因是燃料燃烧不充分(或空气或氧气不足).此时就需要增大(填“增大”或“减小”)灶具的进风口.
(2)如图2、图3分别表示1kg不同燃料燃烧产生CO2和SO2的质量.
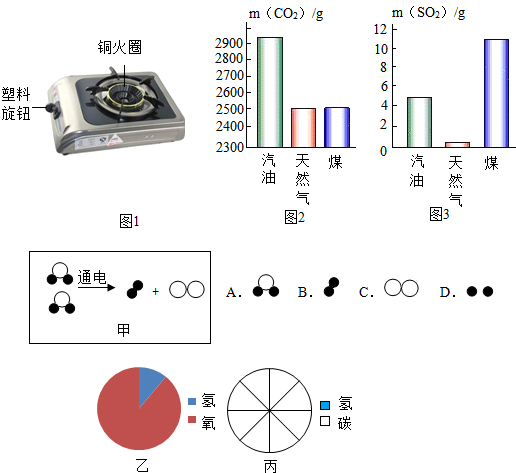
①其中较清洁的燃料是天然气,使用煤作燃料时最易形成酸雨.
②减少温室气体二氧化碳的排放,可以将二氧化碳进行转化.如图为该反应的微观示意图,根据图示回答下列问题.
以上4种物质中属于氧化物的是AC(填字母序号); 该反应中A、C两种物质的质量比是11:9.
(3)①图甲是水分子电解模型图,根据质量守恒定律可判断该模型图中缺少了B;
②图乙表示水中各元素质量分数模型,请模仿该图,在图丙中建立甲烷(CH4)中各元素质量分数模型.
(1)如图1是燃气灶的图片:图片中含有的有机合成材料是塑料旋钮.当燃气灶的火焰呈现黄色或橙色,锅底出现黑色,其原因是燃料燃烧不充分(或空气或氧气不足).此时就需要增大(填“增大”或“减小”)灶具的进风口.
(2)如图2、图3分别表示1kg不同燃料燃烧产生CO2和SO2的质量.

①其中较清洁的燃料是天然气,使用煤作燃料时最易形成酸雨.
②减少温室气体二氧化碳的排放,可以将二氧化碳进行转化.如图为该反应的微观示意图,根据图示回答下列问题.
| 反应前 | 反应后 | 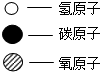 | ||
| A | B | C | D | |
 |  |  |  | |
(3)①图甲是水分子电解模型图,根据质量守恒定律可判断该模型图中缺少了B;
②图乙表示水中各元素质量分数模型,请模仿该图,在图丙中建立甲烷(CH4)中各元素质量分数模型.
19.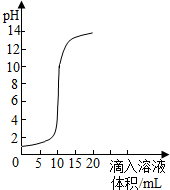 如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列说法不正确的是( )
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列说法不正确的是( )
 如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列说法不正确的是( )
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列说法不正确的是( )| A. | 该实验是将氢氧化钠溶液滴入盐酸中 | |
| B. | 氢氧化钠溶液和盐酸恰好反应时,溶液PH=7 | |
| C. | 当滴加入20ml溶液时,再滴加石蕊试剂,溶液呈红色 | |
| D. | 当pH=12时,所得溶液的溶质为NaCl和NaOH |
 “中心物质法”是化学复习过程中常用的一种学习方法,它是以一种物质为核心,通过发散思维,建立物质间的相互联系,从而把零碎的化学知识连成网络.已知A、B、C、D、E是初中化学常见的五种不同物质,A、E均是空气中常见的气体,B、D组成元素完全相同(说明:“-”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能向箭头所指方向转化,“←→”表示相连的两种物质能相互转化)试根据如图所示的关系回答下列问题:
“中心物质法”是化学复习过程中常用的一种学习方法,它是以一种物质为核心,通过发散思维,建立物质间的相互联系,从而把零碎的化学知识连成网络.已知A、B、C、D、E是初中化学常见的五种不同物质,A、E均是空气中常见的气体,B、D组成元素完全相同(说明:“-”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能向箭头所指方向转化,“←→”表示相连的两种物质能相互转化)试根据如图所示的关系回答下列问题: 如图是二氧化碳的知识网络图(反应条件已略去).
如图是二氧化碳的知识网络图(反应条件已略去). 人们日常生活用水必须经过一系列的净化处理才能使用,请你回答:
人们日常生活用水必须经过一系列的净化处理才能使用,请你回答: