题目内容
6.如图所示实验操作不正确的是( )| A. | 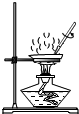 蒸发 | B. |  铁丝在O2中燃烧 | C. |  称量食盐固体 | D. | 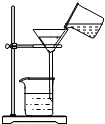 过滤 |
分析 A、根据蒸发操作的注意事项进行分析判断.
B、根据铁丝在氧气中燃烧的实验注意事项,进行分析判断.
C、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
D、过滤液体时,注意“一贴、二低、三靠”的原则.
解答 解:A、蒸发时,应用玻璃棒不断搅拌,以防液体受热不均匀,造成液体飞溅,图中所示操作正确.
B、铁丝在O2中燃烧时,为防止生成物熔化溅落下来使瓶底炸裂,集气瓶的底部应放少量的水或铺一层细沙,图中所示装置正确.
C、托盘天平的使用要遵循“左物右码”的原则,图中所示装置正确.
D、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、漏斗下端没有紧靠在烧杯内壁上,图中所示操作错误.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
14.科学家调查发现边远山村的人各种心血管疾病等现代慢性病的发病率比较低.分析他们的膳食结构,吃的植物性食物较多,尤其是各种蔬菜.由此推断,食物中哪种营养素可能对预防心血管疾病的发生具有重要作用( )
| A. | 糖类 | B. | 蛋白质 | C. | 纤维素 | D. | 无机盐 |
1.甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取10g样品溶于一定量的水中得到50g溶液,再分别加入质量不同,溶质质量分数均为10%的氢氧化钠溶液,反应得到沉淀的实验数据如表:
试回答下列问题:
(1)上述实验中,丙同学所用的氢氧化钠溶液一定过量.
(2)求样品中氯化镁的质量(写出计算过程).$\frac{10g-9.5g+11.7g}{50g+80g-5.8g}$
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数.(结果精确到0.01%)
| 甲 | 乙 | 丙 | |
| 加入氢氧化钠溶液质量 (g) | 70 | 80 | 90 |
| 反应得到沉淀的质量 (g) | 5 | 5.8 | 5.8 |
(1)上述实验中,丙同学所用的氢氧化钠溶液一定过量.
(2)求样品中氯化镁的质量(写出计算过程).$\frac{10g-9.5g+11.7g}{50g+80g-5.8g}$
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数.(结果精确到0.01%)
18.MP2.5中文名为“细微颗粒物”,细颗粒物只是地球大气成分中含量很少的组分,但它对空气质量和能见度等有重要的影响.下列不属于细微颗粒物来源的是( )
| A. | 绿色植物的花粉 | B. | 火山爆发出的火山灰 | ||
| C. | 光合作用产生的氧气 | D. | 森林大火产生的灰尘 |
15.二十一世纪是海洋开发与利用的世纪,我市规划确立了“蓝色经济”发展战略,海洋化学资源的综合利用将是重点发展领域之一.以下是某研究性学习小组在探究海水综合利用中遇到的问题,请你参与解决并填空:
问题一、海水制镁过程中如何富集镁离子?
甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳.
乙:高温加热蒸发海水后,加入石灰乳.
丙:向晒盐后的卤水中,加入石灰乳.
通过分析比较,你认为丙的设想最为经济合理(选填“甲”、“乙”或“丙”).
问题二、粗盐纯化过程中如何除去可溶性杂质?
粗盐中含有硫酸钠、氯化钙等杂质.提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是完全除尽硫酸根离子;再加过量的碳酸钠溶液,除去杂质阳离子;滤去沉淀,向滤液中加入稀盐酸,将溶液的pH调为7,即得到精盐水.
问题三、海水“制碱”的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中含有碳酸钠和氢氧化钠;
丙的猜想:样品中只含有氢氧化钠.
他们做出上述三种猜想的科学依据是化学反应前后元素的种类不变.
【实验、记录与分析】
问题一、海水制镁过程中如何富集镁离子?
甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳.
乙:高温加热蒸发海水后,加入石灰乳.
丙:向晒盐后的卤水中,加入石灰乳.
通过分析比较,你认为丙的设想最为经济合理(选填“甲”、“乙”或“丙”).
问题二、粗盐纯化过程中如何除去可溶性杂质?
粗盐中含有硫酸钠、氯化钙等杂质.提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是完全除尽硫酸根离子;再加过量的碳酸钠溶液,除去杂质阳离子;滤去沉淀,向滤液中加入稀盐酸,将溶液的pH调为7,即得到精盐水.
问题三、海水“制碱”的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中含有碳酸钠和氢氧化钠;
丙的猜想:样品中只含有氢氧化钠.
他们做出上述三种猜想的科学依据是化学反应前后元素的种类不变.
【实验、记录与分析】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全溶解,再加入过量氯化钡溶液; | 生成白色的沉淀 | 丙的猜想不成立 |
| 2 | 取步骤1反应后的溶液与试管中滴加无色的酚酞试液 | 无明显现象 | 只有甲的猜想成立 |
16.下列判断正确的是( )
| A. | 使酚酞试液变红的溶液是碱性溶液 | |
| B. | PH越小,酸性越弱 | |
| C. | 证明溶液里面含有Cl-,只需要加入AgNO3溶液 | |
| D. | PH<7的雨水叫酸雨 |
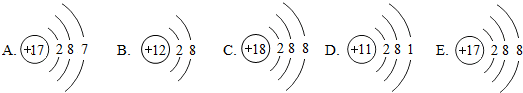
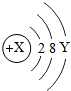 为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.
为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.