题目内容
11.某工厂生产的工业纯碱中含有氯化钠,取55g该工业纯碱,向其中加入269.5g稀盐酸,恰好完全反应,生成22g二氧化碳,求:(1)工业纯碱中碳酸钠的质量分数.(计算结果保留到0.1%)
(2)反应后溶液中溶质的质量分数.
分析 (1)根据二氧化碳的质量可求出碳酸钠的质量,可求出纯碱样品中碳酸钠的质量分数;
(2)根据二氧化碳可求出生成氯化钠的质量,依据碳酸钠的质量可求出原混合物中氯化钠的质量,反应后溶液的质量=反应前各组份的质量之和-气体的质量,并计算所得溶液的溶质质量分数.
解答 解:设55g纯碱样品中碳酸钠的质量为x,生成的氯化钠质量是y,
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 117 44
x y 22g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{22g}$
x=53g
y=58.5g
则该纯碱样品中碳酸钠的质量分数为:$\frac{53g}{55g}$×100%=96.4%;
原混合物中氯化钠的质量是55g-53g=2g,反应后溶液的质量是55g+269.5g-22g=302.5g,则反应后所得所得溶液中NaCl的质量分数:$\frac{2g+58.5g}{302.5g}$×100%=20%.
故答案为:(1)96.4%;
(2)20%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
2.下列区分物质的方法不正确的是( )
| A. | 用酚酞溶液区分稀盐酸和食盐水 | |
| B. | 用燃着的木条区分氧气和二氧化碳 | |
| C. | 用肥皂水区分硬水和软水 | |
| D. | 用水区分硝酸铵固体和氢氧化钠固体 |
16.如图所示实验操作正确的是( )
| A. | 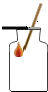 二氧化碳验满 | B. |  测定溶液pH | ||
| C. | 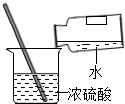 稀释浓硫酸 | D. | 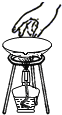 移走加热后的蒸发皿 |
3.中学生应掌握一些安全常识,下列有关做法或说法正确的是( )
| A. | 霉变的大米蒸煮后可以放心食用 | |
| B. | 为了用电安全,不接触低压带电体,不靠近高压带电体 | |
| C. | 燃烧着的酒精灯被碰倒后,要尽快吹灭,以防止洒出的酒精燃烧起来 | |
| D. | 为防止接入电路中用电器的总功率过大,烧断保险丝而引发停电事故,要换用较粗的保险丝 |
9.下列物质的鉴别方法正确的是( )
| A. | 用澄清石灰水鉴别氢气和一氧化碳 | |
| B. | 用无色酚酞鉴别碳酸钠溶液和氢氧化钠溶液 | |
| C. | 用紫色石蕊溶液鉴别氯化铵溶液和稀盐酸 | |
| D. | 用水鉴别氢氧化钙固体和氢氧化钠固体 |
10. 分别向a、b两支试管中加入形状和大小完全相同的铁片,再向a中加入植物油,均塞上橡皮塞,U型玻璃管内为红墨水(开始时两端液面水平),如图所示,放置一段时间后,以下说法错误的是( )
分别向a、b两支试管中加入形状和大小完全相同的铁片,再向a中加入植物油,均塞上橡皮塞,U型玻璃管内为红墨水(开始时两端液面水平),如图所示,放置一段时间后,以下说法错误的是( )
 分别向a、b两支试管中加入形状和大小完全相同的铁片,再向a中加入植物油,均塞上橡皮塞,U型玻璃管内为红墨水(开始时两端液面水平),如图所示,放置一段时间后,以下说法错误的是( )
分别向a、b两支试管中加入形状和大小完全相同的铁片,再向a中加入植物油,均塞上橡皮塞,U型玻璃管内为红墨水(开始时两端液面水平),如图所示,放置一段时间后,以下说法错误的是( )| A. | 植物油用于隔绝氧气和水 | |
| B. | a试管中铁片不被腐蚀,b试管中铁片被腐蚀 | |
| C. | U形玻璃管两端液面变为右低左高 | |
| D. | U形玻璃管两端液面变为左低右高 |
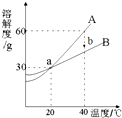 如图是A、B两种物质的溶解度曲线,请回答:
如图是A、B两种物质的溶解度曲线,请回答: