题目内容
5. A~G是初中化学常见的物质,它们之间的关系如图所示,其中①是中和反应,乙是一种红色粉末,“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:
A~G是初中化学常见的物质,它们之间的关系如图所示,其中①是中和反应,乙是一种红色粉末,“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:(1)A的化学式是CaCO3;
(2)B→D的基本反应类型:化合反应;
(3)写出反应①的化学方程式:Ca(OH)2+2HCl═CaCl2+2H2O.
(4)写出反应②的化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 根据A高温分解可推测知:A可能是碳酸钙,①是中和反应,所以D是一种碱,由于氧化钙能与水反应生成碱氢氧化钙;所以B是氧化钙、D是氢氧化钙,F是一种酸,则C是二氧化碳,二氧化碳能与碳反应生成一氧化碳E,根据“乙是一种红色粉末”,一氧化碳能与金属氧化物反应生成金属G,G在氢前时能与酸F反应生成氢气,据此分析解答即可.
解答 解:
根据A高温分解可推测知:A可能是碳酸钙,①是中和反应,所以D是一种碱,由于氧化钙能与水反应生成碱氢氧化钙;所以B是氧化钙D是氢氧化钙,F是一种酸,则C是二氧化碳,二氧化碳能与碳反应生成一氧化碳E,根据“乙是一种红色粉末”,一氧化碳能与金属氧化物反应生成金属G,G在氢前时能与酸F反应生成氢气,乙是一种红色粉末,故G是铁;代入检验,符合题意.
(1)由分析知A可能是碳酸钙,则其化学式为CaCO3;
(2)根据分析,B是氧化钙、D是氢氧化钙,即氧化钙能与水反应生成碱氢氧化钙,故B→D的基本反应类型为化合反应;
(3)①是中和反应:氢氧化钙与稀盐酸的反应,其化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O;
(4)②是氧化铁和一氧化碳的反应,其化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
故答案为:
CaCO3;化合反应; Ca(OH)2+2HCl═CaCl2+2H2O(可多种答案); 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
点评 解答这类框图推断题的关键是找好突破口,缩小范围之后根据已推出的作为源头根据题中信息导出其他的物质;做推断题要根据信息敢于假设.

练习册系列答案
相关题目
7.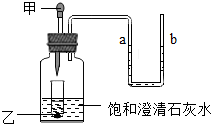 如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中).当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U形管中的a液面降低、b液面升高了.请你根据以上现象分析,下列说法不正确的是( )
如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中).当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U形管中的a液面降低、b液面升高了.请你根据以上现象分析,下列说法不正确的是( )
 如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中).当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U形管中的a液面降低、b液面升高了.请你根据以上现象分析,下列说法不正确的是( )
如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中).当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U形管中的a液面降低、b液面升高了.请你根据以上现象分析,下列说法不正确的是( )| A. | 甲、乙可能分别是稀硫酸和碳酸钠 | |
| B. | 甲、乙有可能分别是水和硝酸铵 | |
| C. | 甲、乙可能分别是氧化钙和水 | |
| D. | 石灰水变浑浊,不可能是发生了物理变化 |
13.下列变化中,属于物理变化的是( )
| A. | 面包发霉 | B. | 汽油燃烧 | C. | 海水晒盐 | D. | 大米酿酒 |
17.如图所示的化学实验基本操作中,正确的是( )
| A. | 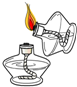 点燃酒精灯 | B. | 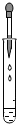 滴加液体 | ||
| C. | 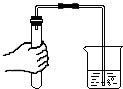 检查装置的气密性 | D. |  加热固体 |
15.在化学实验室,小刚和小强意外发现实验桌上有一瓶敞口放置的氢氧化钠固体,他们对这瓶氢氧化钠固体是否变质进行了如下实验探究:
[提出问题]
这瓶氢氧化钠固体是否变质?
氢氧化钠露置在空气中会发生变质.变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
[实验探究]
为检验这瓶氢氧化钠固体是否变质,小刚设计了如下实验方案:
取少量样品加适量蒸馏水配成溶液后,滴入几滴酚酞溶液,若观察到溶液变红色,证明该瓶氢氧化钠固体没有变质.小强认为方案不正确,理由是:碳酸钠溶液显碱性,也能使酚酞溶液变红.
请你设计另外一个方案,证明该瓶氢氧化钠固体已经变质,并完成以下实验报告:
[提出问题]
这瓶氢氧化钠固体是否变质?
氢氧化钠露置在空气中会发生变质.变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
[实验探究]
为检验这瓶氢氧化钠固体是否变质,小刚设计了如下实验方案:
取少量样品加适量蒸馏水配成溶液后,滴入几滴酚酞溶液,若观察到溶液变红色,证明该瓶氢氧化钠固体没有变质.小强认为方案不正确,理由是:碳酸钠溶液显碱性,也能使酚酞溶液变红.
请你设计另外一个方案,证明该瓶氢氧化钠固体已经变质,并完成以下实验报告:
| 实验步骤 | 实验现象及结论 |
| 取少量样品加适量蒸馏水配成溶液后, 滴加适量稀盐酸 | 有气泡生成,证明该氢氧化钠已变质 |
