题目内容
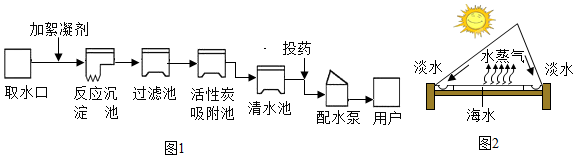
7.水是地球表面覆盖着最多的物质,也是生命活动不可缺少的物质.城镇自来水厂生产流程可用图1表示:①明矾作絮凝剂是因为与水反应生成氢氧化铝胶状物,氢氧化铝的化学式为Al(OH)3;
②投药(多为ClO2)的作用是杀菌消毒.
③自然界的水多含有杂质,含有较多可溶性钙、镁化合物的水通常称为硬水,生活中将硬水软化的方法是煮沸;
④海水淡化可缓解水资源匮乏的问题,如图2为海水淡化装置示意图,请从能源角度指出其优点,节约能源水变成水蒸气的过程中,不发生变化的是AB(填字母序号)
A.分子质量 B.分子种类 C.分子间隔
分析 ①根据物质化学式的写法解答;
②根据自来水厂生产流程中各装置的特点、作用分析回答;
③根据常见的软化硬水的简易办法回答;
④根据水变成水蒸气的过程中是物理变化解答;
解答 解:
①氢氧化铝的化学式为:Al(OH)3;
②投药(多为ClO2)的作用是杀菌消毒.
③自然界的水多含有杂质.含有较多可溶性钙、镁化合物的水通常称为硬水,一种软化硬水的简易办法是:煮沸,煮沸能减少水中钙镁的化合物的量.
④水变成水蒸气的过程需加热耗费能源;从海水中获取淡水节约能源.水变成水蒸气的过程中,是物理变化,不发生变化的是分子质量 和分子种类.
答案:
①Al(OH)3;
②杀菌消毒;
③煮沸;
④节约能源;AB.
点评 本题以净化水为中心,同时考查的还有过滤的操作、硬水和软水的区别和转化方法以及物理变化和化学变化的判断,解题时要针对题目的具体情况,结合所学习的基础知识,经过仔细分析后再作回答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.固体混合物A是由Mg、CuO、Na2SO4、Na2CO3、BaCl2、BaSO4中的几种混合而成,为确定其成分,进行如图实验.(假设每步反应均恰好完全反应)下面推断不正确的是( )
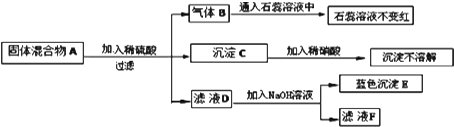

| A. | 由气体B可推原固体混合物A中一定含有Mg,一定不含Na2CO3. | |
| B. | 沉淀C一定为BaSO4,由此可推原固体混合物A中一定含有BaCl2和Na2SO4 | |
| C. | 滤液D中一定含有的溶质是MgSO4和CuSO4 | |
| D. | 固体A的组成可能有6种. |
15.下列各组溶液中不用其他试剂,仅用组内物质相互反应就能区别开来的是( )
| A. | NaOH、CuSO4、MgCl2 | B. | Na2SO4、BaCl2、Na2CO3 | ||
| C. | KNO3、CuSO4、NaCl | D. | NaNO3、BaCl2、KCl |
12.某校化学实验小组准备学习探究合金中某成分的测定方法.
【提出问题】如何利用黄铜(Cu-Zn合金)与稀硫酸反应来测定黄铜中锌的含量.
【实验设计】通过下列两个实验分别测定H2的质量和体积:
【分析表达】(1)实验I中,将小烧杯中的所有稀硫酸分几次加入到大烧杯中,并不断搅拌,判断大烧杯中药品完全反应的实验现象是不再产生气泡;
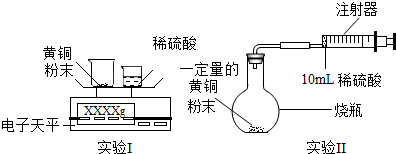
(2)实验II中,注射器的作用是注射10mL稀硫酸和收集氢气.
该实验操作是:先连接好装置,再检查装置气密性(填操作名称),该操作的具体方法是将注射器活塞向内(左)推动一段距离,松手后注射器活塞回到原来的位置;然后装好药品,最后将10mL稀硫酸快速推入烧瓶中,若稀硫酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀硫酸难以完全推入烧瓶中或仪器连接处脱落.
【实验记录】(3)已知实验I反应前的总质量[m(大烧杯+黄铜粉末)+m(小烧杯+稀硫酸)】,要计算生成H2的质量,至少还需要的数据是AC(填字母);
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)实验II的实验数据记录如下(表中数据在相同温度、相同压强条件下测定):
根据以上实验过程和数据综合分析,最终生成H2的体积是80.0 mL.
【数据处理】(5)若实验II中黄铜的质量是5g,lOmL稀硫酸过量,氢气的密度为0.09g/lOOOmL.利用上表数据可计算出该黄铜中锌的质量分数为4.7%(精确至0.1%)
【反思评价】(6)黄铜的颜色非常接近18K金,有不法分子用黄铜冒充18K金行骗.你知道怎样区别黄铜和黄金吗?简要说说鉴别方法方法一:分别向黄铜和黄金上滴加稀盐酸或稀硫酸,产生气泡的是黄铜,不产生气泡的是黄金;
方法二:取黄铜和黄金分别在酒精灯火焰上灼烧,表面变黑的是黄铜,无明显现象的是黄金.
【提出问题】如何利用黄铜(Cu-Zn合金)与稀硫酸反应来测定黄铜中锌的含量.
【实验设计】通过下列两个实验分别测定H2的质量和体积:
【分析表达】(1)实验I中,将小烧杯中的所有稀硫酸分几次加入到大烧杯中,并不断搅拌,判断大烧杯中药品完全反应的实验现象是不再产生气泡;

(2)实验II中,注射器的作用是注射10mL稀硫酸和收集氢气.
该实验操作是:先连接好装置,再检查装置气密性(填操作名称),该操作的具体方法是将注射器活塞向内(左)推动一段距离,松手后注射器活塞回到原来的位置;然后装好药品,最后将10mL稀硫酸快速推入烧瓶中,若稀硫酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀硫酸难以完全推入烧瓶中或仪器连接处脱落.
【实验记录】(3)已知实验I反应前的总质量[m(大烧杯+黄铜粉末)+m(小烧杯+稀硫酸)】,要计算生成H2的质量,至少还需要的数据是AC(填字母);
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)实验II的实验数据记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/mL | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
【数据处理】(5)若实验II中黄铜的质量是5g,lOmL稀硫酸过量,氢气的密度为0.09g/lOOOmL.利用上表数据可计算出该黄铜中锌的质量分数为4.7%(精确至0.1%)
【反思评价】(6)黄铜的颜色非常接近18K金,有不法分子用黄铜冒充18K金行骗.你知道怎样区别黄铜和黄金吗?简要说说鉴别方法方法一:分别向黄铜和黄金上滴加稀盐酸或稀硫酸,产生气泡的是黄铜,不产生气泡的是黄金;
方法二:取黄铜和黄金分别在酒精灯火焰上灼烧,表面变黑的是黄铜,无明显现象的是黄金.
19.下列说法全部正确的是( )
①天然种植的蔬菜,不含任何元素,真正的“绿色”食品
②分离液态空气法制氧气属于分解反应
③某固态物质受热后变为气态物质,该变化可能属于物理变化
④喝了汽水会打嗝,说明温度升高气体的溶解度减小
⑤锌、硒等是人体必须的微量元素,应大量服用含有这些元素的营养补剂
⑥碱的水溶液通常显碱性,所以呈碱性的溶液一定是碱溶液
⑦因为MnO2能加快H2O2的分解,所以催化剂一定加快化学反应速率.
①天然种植的蔬菜,不含任何元素,真正的“绿色”食品
②分离液态空气法制氧气属于分解反应
③某固态物质受热后变为气态物质,该变化可能属于物理变化
④喝了汽水会打嗝,说明温度升高气体的溶解度减小
⑤锌、硒等是人体必须的微量元素,应大量服用含有这些元素的营养补剂
⑥碱的水溶液通常显碱性,所以呈碱性的溶液一定是碱溶液
⑦因为MnO2能加快H2O2的分解,所以催化剂一定加快化学反应速率.
| A. | 只有①②③ | B. | 都正确 | C. | 只有③和④正确 | D. | ②③④正确 |
16.只用C、CO、O2、CuO、CaCO3、稀HCl六种物质,进行单一或两两反应,可写出生成二氧化碳的化学方程式有( )
| A. | 6个 | B. | 5个 | C. | 4个 | D. | 3个 |
17.下列过程中主要只涉及物理变化的是( )
| A. | 用稀盐酸除铁锈 | |
| B. | 用灼烧法鉴别羊毛和合成纤维 | |
| C. | 废气屮的二氧化硫形成酸雨 | |
| D. | 用酒精浸泡紫罗兰花自制酸碱指示剂 |